题目内容
在恒温恒容的密闭容器中,发生反应3A(g)+B(g)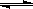 xC(g)。
xC(g)。
Ⅰ、将3molA和2molB在一定条件下反应,达平衡时C的体积分数为a;
Ⅱ、若起始时A、B、C投入的物质的量分别为n(A)、n(B)、n(C),平衡时C的体积分数也为a。下列说法正确的是
A、若Ⅰ达平衡时,A、B、C各增加1mol,则B的转化率将一定增大
B、若向Ⅰ平衡体系中再加入3molA和2molB,C的体积分数若大于a,可断定x>4
C、若x=2,则Ⅱ体系起始物质的量应当满足3 n(B) =n(A)+3
D、若Ⅱ体系起始物质的量当满足3 n(C) +8n(A)==6 n(B)时,可断定x=4
【答案】
D
【解析】这是恒温恒容条件下的等效平衡,即无论如何进行配比,只要把一端按不可逆反应形式完全转化为另一端的物质后,相当于完全等同的起始量即可。A不一定的,把C完全转化为反应物,则此时A和B的物质的量分别是(4+1/x)mol和(3+1/x)mol。如果x的值能够保证让这两个式子的比例保持3︰2不变化,则化率可以不变;B相当于在原平衡的基础上增大压强,平衡向正反应方向进行,所以x小于4,B不正确;选项C中要满足平衡等效,则n(A)+3n(C)/2=3和n(B)+n(C)/2=2,所以3 n(B) =n(A)+3,即该式是恒成立的,C不正确。如果x=4,则只要把一端按不可逆反应形式完全转化为另一端的物质后,A和B的物质的量之比满足3︰2即可。即[n(A)+3n(C)/4]/[n(B)+n(C)/4[=3/2,解得3 n(C) +8n(A)==6 n(B),所以选项D正确,答案选D。

练习册系列答案
相关题目
在恒温恒容的密闭容器中,有可逆反应2NO(g)+O2(g)?2NO2(g).下列不能说明该反应已达到化学平衡状态的是( )
| A、反应容器中压强不随时间变化而变化 | B、混合气体颜色保持不变 | C、混合气体的密度保持不变 | D、各物质的物质的量浓度保持不变 |
 2NH3,,平衡后,测得反应放出的热量为18.4kJ,混合气体总的物质的量为3.6mol,容器内的压强变为原来的90%.又知N2和H2的转化率相同.
2NH3,,平衡后,测得反应放出的热量为18.4kJ,混合气体总的物质的量为3.6mol,容器内的压强变为原来的90%.又知N2和H2的转化率相同.