题目内容
25 ℃时,关于浓度均为0.2 mol/L的Na2CO3和NaHCO3溶液的说法不正确的是( )
| A.两溶液中均存在电离平衡和水解平衡 |
| B.两溶液分别加水稀释后,pH和KW均减小 |
| C.两溶液中均存在c(OH-)+2c(CO32—)+c(HCO3—)=c(Na+)+c(H+) |
| D.c(OH-)前者大于后者 |
B
两溶液中均存在水的电离平衡和盐类的水解平衡,A项正确;KW只与温度有关,温度不变KW不变,B项错误;根据溶液的电中性可知C项正确;CO32—的水解程度要远大于HCO3—的水解程度,故等物质的量浓度的Na2CO3溶液和NaHCO3溶液,c(OH-)前者要大于后者,D项正确

练习册系列答案
相关题目

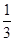 ,加入适量无水乙醇,放置8h以上,经结晶、分离、干燥获得葡萄糖酸锌晶体。分离过程中加入无水乙醇的目的是 。
,加入适量无水乙醇,放置8h以上,经结晶、分离、干燥获得葡萄糖酸锌晶体。分离过程中加入无水乙醇的目的是 。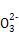 ),且c(Mg2+)·c(C
),且c(Mg2+)·c(C 的硬水,发生的离子反应方程式为Mg2++2HC
的硬水,发生的离子反应方程式为Mg2++2HC CaCO3↓+MgCO3↓+2H2O
CaCO3↓+MgCO3↓+2H2O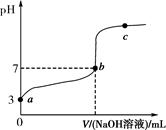
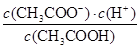 均相等
均相等