题目内容
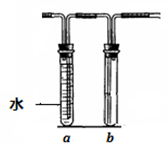
几位同学设计实验观察铜与浓硫酸的反应,检验生成的气体的性质.甲设计了如图所示的装置,在大试管里加入2 mL浓硫酸,用带导管和一个小孔的胶管塞紧,从孔中插入一根铜丝,加热,把产生的气体依次通入品红溶液和石蕊溶液中.

请回答下列问题:
(1)写出铜与浓硫酸反应的化学方程式:________.
(2)试管b中的现象是________,通过试管a、b的现象得出的结论是________.
(3)乙同学认为甲同学的设计不能全面体现SO2的性质,他打算增加试管进行其它实验.以下为增加的试管中盛放的试剂:
A.澄清石灰水
B.KMnO4(aq)
C.氢硫酸
请你帮助乙同学作出选择,在横线上先写出字母,再用文字简单说明实验的目的.
________________
(4)丙同学评价甲同学的实验装置既有优点也有不足,优点是________,不足之处改进的具体措施是________.
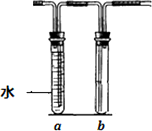
(5)若把上述装置中大试管的浓硫酸换成稀硝酸,试管a和b作如下改变(其中a装满水,b空置),则在大试管中发生的反应的离子方程式为________,试管a的作用是________________.
答案:

练习册系列答案
 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案
相关题目