题目内容
| 元素 | 有关信息 |
| A | 元素主要化合价为-2,原子半径为0.074nm |
| B | 所在主族序数与所在周期序数之差为4,同周期主族元素中原子半径最小 |
| C | 原子半径为0.102nm,其单质在A的单质中燃烧,发出明亮的蓝紫色火焰 |
| D | 最高价氧化物对应水化物,能按1:1电离出电子数相等(10个电子)的阴阳离子 |
| E | 原子半径为0.075nm,最高价氧化物对应水化物与其氢化物组成一种盐X |
(2)画出B的原子结构示意图:
(3)盐X水溶液显
(4)D2CA3的溶液与B的单质能发生氧化还原反应,其反应的离子方程式为
(5)已知E元素的某种氢化物Y与A2的摩尔质量相同,Y在常温下为液态,Y的化学式为
(a)极性键 (b)非极性键 (c)离子键.
A元素主要化合价为-2,原子半径为0.074nm,则A处于第ⅥA族;
C原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰,则C为S元素,A为O元素;
B所在主族序数与所在周期序数之差为4,满足该条件元素为O或Cl,由于A为O元素,则B为Cl元素.
D最高价氧化物的水化物,为酸或碱,能按1:1电离出电子数相等的阴、阳离子,则D为Na元素,
E原子半径为0.075n m,最高价氧化物的水化物与其氢化物组成一种盐X,则E为N元素,X为NH4NO3.
A元素主要化合价为-2,原子半径为0.074nm,则A处于第ⅥA族;
C原子半径为0.102nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰,则C为S元素,A为O元素;
B所在主族序数与所在周期序数之差为4,满足该条件元素为O或Cl,由于A为O元素,则B为Cl元素.
D最高价氧化物的水化物,为酸或碱,能按1:1电离出电子数相等的阴、阳离子,则D为Na元素,
E原子半径为0.075n m,最高价氧化物的水化物与其氢化物组成一种盐X,则E为N元素,X为NH4NO3,
(1)由上述分析可知,A为O、B为Cl、C为S、D为Na、E为N,
故答案为:O;Cl;S;Na;N;
(2)Cl原子核外电子数为17,其原子结构示意图为:
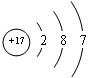 ;Na元素最高价氧化物对应水化物为NaOH,NaOH是离子化合物,由钠离子和氢氧根离子构成,其电子式为
;Na元素最高价氧化物对应水化物为NaOH,NaOH是离子化合物,由钠离子和氢氧根离子构成,其电子式为 .
.故答案为:
 ;
; .
.(3)X为NH4NO3,是强酸弱碱盐,铵根离子水解NH4++H2O?NH3?H2O+H+,溶液呈酸性,
故答案为:酸;NH4++H2O?NH3?H2O+H+;
(4)Cl2具有强氧化性,Na2SO3有较强的还原性,氯气能将亚硫酸根氧化为硫酸根,反应离子方程式为SO32-+Cl2+H2O═SO42-+2H++2Cl-,
故答案为:SO32-+Cl2+H2O═SO42-+2H++2Cl-;
(5)A2的为O2,摩尔质量为32g/mol,所以N元素的氢化物Y的摩尔质量为32g/mol,氢化物Y为N2H4,分子中氮原子与氢原子之间形成极性键,氮原子之间形成非极性键,
故答案为:N2H4;ab.

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案元素代号 | A | B | C | D | E |
原子半径/nm | 0.16 | 0.143 | 0.102 | 0.089 | 0.074 |
主要化合价 | +2 | +3 | +6,-2 | +2 | -2 |
(1)用元素代号标出它们在周期表中对应位置
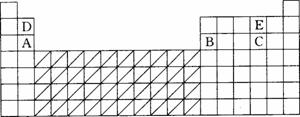
(2)C、E形成化合物为______________(填化学式),周期表有些元素存在“对角线相似”现象,请写出D的单质与强碱溶液反应的离子方程式:______________________;并用电子式表示其氯化物的形成过程____________________________________________________________。
(3)有一类无机化合反应的通式可以表示为:单质+化合物(1)=化合物(2)。请写出满足以下要
求的4个此类无机化合反应的化学方程式:
①所涉及的元素的原子序数都小于30,②4种单质分属4个不同族。
_______________________________________,_______________________________________,
_______________________________________,_______________________________________。
(4)M为金属元素铼(Re),铼是自然界中最后一种被诺达克等三位科学家于1926年发现的元素。他们从数以吨计的含有多种元素的矿石中,通过复杂的工艺一点一滴地富集浓缩,才制得了仅2mg的金属铼。现代工业上采用的方法是:于
①元素铼的原子序数为_____________,铼元素发现如此艰难和时间上如此漫长的原因:
____________________________________________________________________。
②写出现代工业上用氢气冶炼金属铼的化学方程式,并标出电子转移的方向和数目:_____________________________________________________________________。
