题目内容
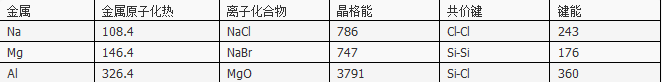
表中原子化热、晶格能、键能的单位都是kJ·mol-1
| 金属 | 金属原子化热 | 离子化合物 | 晶格能 | 共价键 | 键能 |
| Na | 108.4 | NaCl | 786 | Cl-Cl | 243 |
| Mg | 146.4 | NaBr | 747 | Si-Si | 176 |
| Al | 326.4 | MgO | 3791 | Si-Cl | 360 |
则下列说法正确的是
- A.Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量为556.1kJ
- B.Si(s)+2Cl2(g)=SiCl4(g) △H=-602kJ·mol-1
- C.从表中可以看出,氯化钠的熔点比晶体硅高
- D.从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强
B
试题分析:金属原子化热是指 1mol 金属变成气态原子所需要的热量,不能用金属原子化热计算Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量,A项错误;氯化钠与晶体硅的晶体类型不同,所以不能用晶格能和共价键的键能来比较,C项错误;微粒半径越大,共价键也越弱,D项错误;C项:△H="176" kJ·mol-1X2+2X243 kJ·mol-1-360 kJ·mol-1X4="-602" kJ·mol-1,B项正确。
考点:本题考查△H的计算及化学键的强弱、晶体熔点的比较。
试题分析:金属原子化热是指 1mol 金属变成气态原子所需要的热量,不能用金属原子化热计算Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量,A项错误;氯化钠与晶体硅的晶体类型不同,所以不能用晶格能和共价键的键能来比较,C项错误;微粒半径越大,共价键也越弱,D项错误;C项:△H="176" kJ·mol-1X2+2X243 kJ·mol-1-360 kJ·mol-1X4="-602" kJ·mol-1,B项正确。
考点:本题考查△H的计算及化学键的强弱、晶体熔点的比较。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
表中原子化热、晶格能、键能的单位都是kJ·mol-1
|
金属 |
金属原子化热 |
离子化合物 |
晶格能 |
共价键 |
键能 |
|
Na |
108.4 |
NaCl |
786 |
Cl-Cl |
243 |
|
Mg |
146.4 |
NaBr |
747 |
Si-Si |
176 |
|
Al |
326.4 |
MgO |
3791 |
Si-Cl |
360 |
则下列说法正确的是( )
A.Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量为556.1kJ
B.Si(s)+2Cl2(g)=SiCl4(g) △H=-602kJ·mol-1
C.从表中可以看出,氯化钠的熔点比晶体硅高
D.从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强
表中原子化热、晶格能、键能的单位都是kJ·mol-1
|
金属 |
金属原子化热 |
离子化合物 |
晶格能 |
共价键 |
键能 |
|
Na |
108.4 |
NaCl |
786 |
Cl-Cl |
243 |
|
Mg |
146.4 |
NaBr |
747 |
Si-Si |
176 |
|
Al |
326.4 |
MgO |
3791 |
Si-Cl |
360 |
则下列说法正确的是( )
A.Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量为556.1kJ
B.Si(s)+2Cl2(g)=SiCl4(g) △H=-602kJ·mol-1
C.从表中可以看出,氯化钠的熔点比晶体硅高
D.从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强
表中原子化热、晶格能、键能的单位都是kJ·mol-1
| 金属 | 金属原子化热 | 离子化合物 | 晶格能 | 共价键 | 键能 |
| Na | 108.4 | NaCl | 786 | Cl-Cl | 243 |
| Mg | 146.4 | NaBr | 747 | Si-Si | 176 |
| Al | 326.4 | MgO | 3791 | Si-Cl | 360 |
A.Na(s)与Cl2(g)反应生成1molNaCl(s)放出的热量为556.1kJ
B.Si(s)+2Cl2(g)=SiCl4(g) △H=-602kJ·mol-1
C.从表中可以看出,氯化钠的熔点比晶体硅高
D.从表中数据可以看出,微粒半径越大金属键、离子键的越弱,而共价键却越强