题目内容
【题目】某研究性学习小组选用以下装置进行实验设计和探究(图中a、b、c均为止水夹):
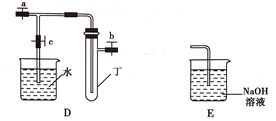
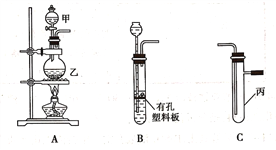
(1)在进行气体制备时,应先检验装置的气密性。将A装置中导管末端密封后,在分液漏斗甲内装一定量的蒸馏水,然后__________________________________________,则证明A装置的气密性良好。
(2)利用E装置能吸收的气体有__________________________________(任写两种即可)。
(3)用锌粒和稀硫酸制备H2时应选用装置________作为发生装置(填所选装置的字母序号),实验时先在稀硫酸中加入少量硫酸铜晶体可使反应速率加快,原因是___________________________。
(4)某同学将A、C、E装置连接后设计实验比较Cl-和S2-的还原性强弱。
①A中玻璃仪器乙的名称为______________________,A装置中发生反应的离子方程式为
_____________________________________________。
②C中说明Cl-和S2-的还原性强弱的实验现象是_______________________________________。
(5)另一同学将B、D、E装置连接后,在B装置中加入铜片和浓硝酸,制取NO2,然后进行NO2气体与水反应的实验,并观察相关现象:
①B装置中发生反应的离子方程式为________________________________________________。
②反应一段时间后D装置中的具支试管丁中收集满NO2气体,若进行NO2气体与水反应的实验,应____________________________________(填对a、b、c三个止水夹进行的操作),然后再适当加热丁。实验现象为____________________________________________________________。
【答案】 打开分液漏斗开关,水不能持续滴下或分液漏斗中液面长时间保持不变 CO2、H2S、Cl2、SO2等气体中任选两种 B Zn和置换出的铜与电解质溶液形成原电池 圆底烧瓶 MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O 产生淡黄色沉淀 Cu+4H++2NO=Cu2++2NO2↑+2H2O 关闭止水夹a、b,打开止水夹c 烧杯中的水进入具支试管中,具支试管中气体颜色变浅
Mn2++Cl2↑+2H2O 产生淡黄色沉淀 Cu+4H++2NO=Cu2++2NO2↑+2H2O 关闭止水夹a、b,打开止水夹c 烧杯中的水进入具支试管中,具支试管中气体颜色变浅
【解析】本题主要考查实验设计和探究。
(1)将A装置中导管末端密封后,在分液漏斗甲内装一定量的蒸馏水,然后打开分液漏斗开关,水不能持续滴下或分液漏斗中液面长时间保持不变,则证明A装置的气密性良好。
(2)利用E装置能吸收的气体有CO2、H2S、Cl2、SO2等酸性气体中任选两种。
(3)用锌粒和稀硫酸制备H2时,反应不需要加热,应选用装置B作为发生装置,实验时先在稀硫酸中加入少量硫酸铜晶体可使反应速率加快,原因是Zn和置换出的铜与电解质溶液形成原电池。
(4)①A中玻璃仪器乙的名称为圆底烧瓶,A装置中发生反应的离子方程式为MnO2+4H++2Cl-![]() Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
②C中说明Cl-和S2-的还原性强弱的实验现象是产生淡黄色沉淀。
(5)①B装置中发生反应的离子方程式为Cu+4H++2NO=Cu2++2NO2↑+2H2O。
②反应一段时间后D装置中的具支试管丁中收集满NO2气体,若进行NO2气体与水反应的实验,应关闭止水夹a、b,打开止水夹c,然后再适当加热丁。实验现象为烧杯中的水进入具支试管中,具支试管中气体颜色变浅。

【题目】工业上利用氯碱工业中的固体废物盐泥(主要成分为Mg(OH)2、CaCO3、BaSO4,除此之外还有NaCl、Al(OH)3、Fe(OH)3、Mn(OH)2等。)与废稀硫酸反应制备七水硫酸镁,产率高,既处理了三废,又有经济效益。其工艺流程如下:
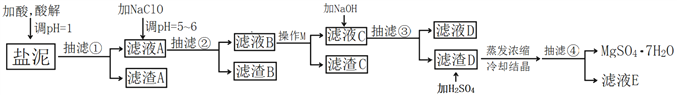
已知:
i)部分阳离子以氢氧化物形式完全沉淀时溶液的pH
沉淀物 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
pH值(完全沉淀) | 10.02 | 8.96 | 3.20 | 4.70 | 11.12 |
ii)两种盐的溶解度图(单位为g/100g水)

根据以上流程图并参考表格pH数据和溶解度图,请回答下列问题。
(1)酸解时,加入的酸为____________,在酸解过程中,想加快酸解速率,请提出两种可行的措施____________、____________。
(2)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式是____________。
(3)本工艺流程多次用到抽滤操作,其优点在于____________,四次抽滤时:抽滤①所得滤渣A的成分为____________、CaSO4;抽滤②所得滤渣B的成分为MnO2、____________、____________;抽滤③所得滤液C中主要杂质阳离子的检验方法是____________;抽滤④将产品抽干。
(4)依据溶解度曲线,操作M应采取的方法是适当浓缩,____________。
(5)每制备1吨MgSO4·7H2O,需要消耗盐泥2吨。若生产过程中的转化率为70%,则盐泥中镁(以氢氧化镁计)的质量分数约为____________。