题目内容
11.设NA为阿伏加德罗常数的数值,下列说法正确的是( )| A. | 常温常压下,16gO3含有NA个氧原子 | |
| B. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| C. | 1mol•L-1MgCl2溶液中含有2NA个Cl- | |
| D. | 1molNa被完全氧化生成Na2O2,失去2NA个电子 |
分析 A、臭氧由氧原子构成;
B、标况下,盐酸为液态;
C、溶液体积不明确;
D、钠反应后变为+1价.
解答 解:A、臭氧由氧原子构成,故16g臭氧中含有的氧原子的物质的量n=$\frac{16g}{16g/mol}$=1mol即NA个,故A正确;
B、标况下,盐酸为液态,不能根据气体摩尔体积来计算其物质的量,故B错误;
C、溶液体积不明确,故溶液中的氯离子的个数无法计算,故C错误;
D、钠反应后变为+1价,故1mol钠反应后失去1mol电子即NA个,与产物无关,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
2.可逆反应:I2(g)+H2(g)?2HI(g),在一定条件下已经达到平衡状态,由于改变浓度、温度、压强等条件中的一个,达到新平衡时,可能引起下列变化,这些变化中能说明平衡一定向正反应方向移动的是( )
①I2(g)浓度减小 ②混合气颜色变浅 ③I2(g)转化率增大 ④HI(g)质量分数增大 ⑤I2(g)+H2(g)质量分数减小.
①I2(g)浓度减小 ②混合气颜色变浅 ③I2(g)转化率增大 ④HI(g)质量分数增大 ⑤I2(g)+H2(g)质量分数减小.
| A. | ①②③ | B. | ②③④ | C. | ③④⑤ | D. | ①③⑤ |
19.已知1g氢气完全燃烧生成水蒸气时放出热量121kJ,且氧气中O=O键键能496kJ/mol,水蒸气中H-O键键能463kJ/mol,则氢气中H-H键键能为( )
| A. | 920kJ/mol | B. | 557kJ/mol | C. | 436kJ/mol | D. | 188kJ/mol |
6.除去下列物质中的少量杂质,所用方法正确的是( )
| 选项 | 物质(括号内为杂质) | 除去杂质的方法 |
| A | KCl(MnO2) | 加水溶解,过滤,洗涤,干燥 |
| B | FeSO4溶液(CuSO4) | 加入适量的锌粉,过滤 |
| C | NaCl溶液(CuCl2) | 加入过量的NaOH溶液,过滤 |
| D | O2(H2O) | 将混合气体通过盛有足量浓硫酸的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |
20.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 5.6 g铁粉在0.1 mol氯气中充分燃烧,转移电子数为0.3NA | |
| B. | 7.8 g Na2S和Na2O2中含有的阴离子数大于0.1NA | |
| C. | 56 g铁片投入足量浓硫酸中生成NA个SO2分子 | |
| D. | 常温常压下,46 g的NO2和N2O4混合气体含有的原子数为3NA |
 现有X、Y、Z三种元素,已知有如下情况:
现有X、Y、Z三种元素,已知有如下情况: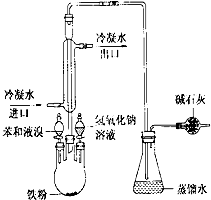 如图是实验室制取溴苯的装置图
如图是实验室制取溴苯的装置图