题目内容
有A、B、C三种可溶性正盐,阴、阳离子各不相同,其阴离子的摩尔质量依次增大(按A、B、C的顺序),将等物质的量的A、B、C溶于水,所得溶液中只含有Fe3+、K+、SO42-、NO3-、Cl-五种离子(不考虑难溶物自身的溶解),同时生成一种阴、阳离子个数比为1:1的白色沉淀。请回答下列问题:
(1)经检验,三种正盐中还含有下列选项中的一种离子,该离子是________.
A.Na+ B.Mg2+ C.Cu2+ D.Ag+
(2)三种正盐的化学式分别是:A ,B ,C
(3) A、B、C同时溶于水时反应的离子方程式为
(1) D(1分)
(2) FeCl3,AgNO3,K2SO4(各2分)
(3) Ag++Cl-=AgCl↓(2分)
解析试题分析:生成一种阴、阳离子个数比为1:1的白色沉淀,从给出的5种离子少了一种阳离子说明完全沉淀,白色沉淀不可能是硫酸盐(因为等物质的量正盐,如果是硫酸盐那么硫酸根离子就没有剩余)只能是氯化银,又根据阴、阳离子各不相同,其阴离子的摩尔质量依次增大(按A、B、C的顺序)B只能是硝酸银,氯离子有剩余所以A应是氯化铁,C既是硫酸钾。
考点:本题考查离子反应和定量的分析。

 通城学典默写能手系列答案
通城学典默写能手系列答案在强酸性溶液中,下列离子组能大量共存且溶液为澄清透明的是
| A.K+、Na+、CO32-、MnO4- | B.Na+、K+、Cl-、HCO3- |
| C.Na+、Cu2+、SO42-、NO3- | D.Ba2+、SO42-、NO3-、K+ |
下列说法及对应的离子方程式均正确的是
A.铁溶于稀HNO3,溶液变黄色:3Fe + 8H+ + 2NO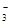 = 3Fe2+ + 2NO↑ + 4H2O = 3Fe2+ + 2NO↑ + 4H2O |
B.用惰性电极电解AlCl3溶液:Al3+ + 3Cl- + 3H2O  Al(OH)3↓ + 3/2H2↑ + 3/2Cl2↑ Al(OH)3↓ + 3/2H2↑ + 3/2Cl2↑ |
C.用酚酞作指示剂,在Na2CO3溶液中滴入乙酸溶液:CO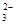 + 2CH3COOH = 2CH3COO- + H2O + CO2↑ + 2CH3COOH = 2CH3COO- + H2O + CO2↑ |
D.在K2Cr2O7溶液中滴入NaOH溶液,溶液变为橙色:Cr2O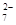 (橙)+ H2O (橙)+ H2O  2CrO 2CrO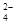 (黄)+2H+ (黄)+2H+ |
常温下,下列各组离子在指定溶液中能大量共存的是
| A.pH=1的溶液中:Fe2+、NO3-、Na+、SO42- |
| B.水电离出的c(H+) =10-12mol/L的溶液中:Ca2+、K+、Cl-、HCO3- |
| C.c(H+)/c(OH-)=1012的水溶液中:NH4+、Al3+、NO3-、Cl- |
| D.c(Fe3+) =0.1mol/L的溶液中:K+、ClO-、SO42-、SCN- |
某工业废水含有下列离子中的5种,K+、Cu2+、Al3+、Fe2+、Cl-、CO32-、NO3-、SO42-,且各种离子的物质的量浓度相等。甲同学欲探究废水的组成,进行了如下实验:
①用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃观察无紫色火焰。
②另取溶液加入足量稀盐酸,有无色气体生成,该无色气体遇空气变成红棕色,此时溶液依然澄清,且溶液中阴离子种类不变。
③另取溶液加入BaCl2溶液,有白色沉淀生成。
根据上述实验,以下推测正确的是:( )
| A.溶液中难以确定Al3+的存在与否 |
| B.原溶液中所含的离子为:Cu2+、Fe2+、Cl-、NO3-、SO42- |
| C.步骤②中可以确定Fe2+、NO3-的存在,不能确定其它离子的存在 |
| D.步骤③中的白色沉淀为2种钡盐 |
在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是( )
| A.Mg2+.Na+.SO42—.Cl- | B.Na+.Cu2+.SO42—.NO3- |
| C.Na+.K+.SO32—.Cl- | D.Ba2+.HCO3—-.ClO—.K+ |
某强碱性溶液中,能大量共存的离子组是
| A.K+、Na+、AlO2-、SO42- | B.K+、Na+、ClO-、S2- |
| C.Na+、K+、SO42-、HCO3- | D.Ca2+、K+、NO3-、I- |
用可溶性钡盐检验SO42-离子的存在时,先在待测溶液中加入盐酸,其作用是 ( )
| A.形成较多的白色沉淀 |
| B.形成的沉淀纯度更高 |
| C.排除SO42- 以外的其它阴离子及Ag+的干扰 |
| D.排除Ba2+ 以外的其它阳离子的干扰 |
下列离子方程式表达正确的是
| A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O |
B.小苏打溶液呈碱性的原因:HCO3-+H2O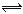 H3O++CO32- H3O++CO32- |
| C.溴化亚铁溶液中通入足量氯气:2Fe2++ 4Br-+ 3Cl2 = 2Fe3++2 Br2 + 6Cl- |
| D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:NH4++Al3++2SO42-+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3·H2O+2H2O |