题目内容
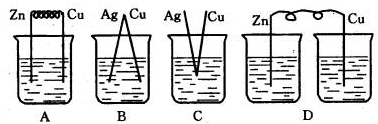
(1)用铜和硫酸铜、银和硝酸银溶液设计一个原电池,电池的负极是______,正极电极反应式是:______.
(2)已知某电池的负极反应为:Cd-2e-+2OH-═Cd(OH)2,正极反应为:NiO(OH)2+2e-+H2O═Ni(OH)2+2OH-.则该电池的电解质溶液可能为______,总反应的化学方程式______.
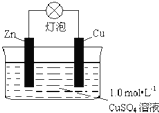
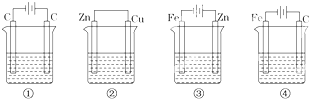
(3)用惰性电极电解稀硫酸、NaOH溶液、NaCl溶液、CuSO4溶液,试写出:电解稀硫酸的阳极反应式______,电解NaOH溶液的阴极反应式______,电解NaCl溶液的总反应化学方程式______,电解CuSO4溶液总反应的离子方程式______.
(2)已知某电池的负极反应为:Cd-2e-+2OH-═Cd(OH)2,正极反应为:NiO(OH)2+2e-+H2O═Ni(OH)2+2OH-.则该电池的电解质溶液可能为______,总反应的化学方程式______.
(3)用惰性电极电解稀硫酸、NaOH溶液、NaCl溶液、CuSO4溶液,试写出:电解稀硫酸的阳极反应式______,电解NaOH溶液的阴极反应式______,电解NaCl溶液的总反应化学方程式______,电解CuSO4溶液总反应的离子方程式______.
(1)铜比银活泼,在铜、银原电池中铜为负极,正极发生还原反应,阴离子得到电子被还原,电极方程式为2Ag-2e-═2Ag+,
故答案为:铜;2Ag-2e-═2Ag+;
(2)正负极电极方程式相加可得总反应式为Cd+NiO(OH)2+H2O═Cd(OH)2+Ni(OH)2,Cd(OH)2和Ni(OH)2只能存在碱性溶液中,则应为KOH或NaOH,
故答案为:KOH;Cd+NiO(OH)2+H2O═Cd(OH)2+Ni(OH)2;
(3)电解硫酸溶液,氧气发生氧化反应生成氧气,电极方程式为4OH--4e-═2H2O+O2↑;电解氢氧化钠溶液,阴极发生还原反应生成氢气,电极方程式为2H++2e-═H2↑;电解NaCl溶液可得到氯气、氢气和氢氧化钠,电解总方程式为2NaCl+2H2O
2NaOH+H2↑+Cl2↑,电解硫酸铜溶液生成铜、氧气和硫酸,总方程式为 2Cu2++2H2O
2Cu+4H++O2↑,
故答案为:4OH--4e-═2H2O+O2↑;2H++2e-═H2↑;2NaCl+2H2O
2NaOH+H2↑+Cl2↑;2Cu2++2H2O
2Cu+4H++O2↑.
故答案为:铜;2Ag-2e-═2Ag+;
(2)正负极电极方程式相加可得总反应式为Cd+NiO(OH)2+H2O═Cd(OH)2+Ni(OH)2,Cd(OH)2和Ni(OH)2只能存在碱性溶液中,则应为KOH或NaOH,
故答案为:KOH;Cd+NiO(OH)2+H2O═Cd(OH)2+Ni(OH)2;
(3)电解硫酸溶液,氧气发生氧化反应生成氧气,电极方程式为4OH--4e-═2H2O+O2↑;电解氢氧化钠溶液,阴极发生还原反应生成氢气,电极方程式为2H++2e-═H2↑;电解NaCl溶液可得到氯气、氢气和氢氧化钠,电解总方程式为2NaCl+2H2O
| ||
| ||
故答案为:4OH--4e-═2H2O+O2↑;2H++2e-═H2↑;2NaCl+2H2O
| ||
| ||

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目