��Ŀ����
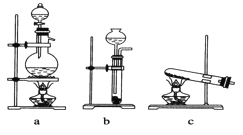
����Ŀ����(N2H4)�ֳ��������ǻ�����õĸ���ȼ�ϣ�������ΪҺ�壬���������ģ����ͼ��ʾ��������˫��ˮ������Ӧ N2H4��2H2O2��N2��4H2O���� NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A.N2H4���ڹ��ۻ����������ֻ���м��Թ��ۼ�
B.��״���£�22.4 L N2H4�к��е�ԭ������Ϊ 6NA
C.��״���£�3.2 g N2H4�к��й��ۼ�������Ϊ 0.6NA
D.������ 3.6g H2O����������Ӧת�Ƶ��ӵ���ĿΪ 0.2NA
���𰸡�D
��������
A. N2H4���ڹ��ۻ����������N-N���ǷǼ��Թ��ۼ�����A����
B.��״������ΪҺ�壬22.4 L N2H4�����ʵ�������1mol����B����
C. N2H4�����к���5�����ۼ���3.2 g N2H4�к��й��ۼ�������Ϊ![]() 0.5NA����C����
0.5NA����C����
D. N2H4��2H2O2��N2��4H2O��H2O2���������������� 3.6g H2O������0.1molH2O2��ת�Ƶ��ӵ���ĿΪ 0.2NA����D��ȷ��
ѡD��

��ϰ��ϵ�д�
 ��ʱѵ���������������ϵ�д�
��ʱѵ���������������ϵ�д� �ƸԾ���Ȥζ����ϵ�д�
�ƸԾ���Ȥζ����ϵ�д� ����С����ҵ��ϵ�д�
����С����ҵ��ϵ�д�
�����Ŀ