题目内容
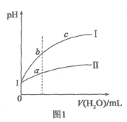
【题目】向20mLNaOH溶液中逐滴加入![]() 醋酸溶液,滴定曲线如图所示。下列判断正确的是
醋酸溶液,滴定曲线如图所示。下列判断正确的是
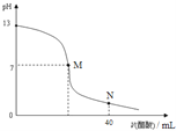
A.在M点,两者恰好反应完全
B.滴定前,酸中![]() 等于碱中
等于碱中![]()
C.NaOH溶液的物质的量浓度为![]()
![]()
D.在N点,c(CH3COO-)> c(Na+)>c(H+)> c(CH3COOH)
【答案】C
【解析】
醋酸体积为0时,还没开始滴定,pH=13,说明该NaOH溶液中,c(H+)=10-13mol/L,c(OH-)=![]() =0.1mol/L,所以,c(NaOH)= 0.1mol/L;
=0.1mol/L,所以,c(NaOH)= 0.1mol/L;
醋酸和NaOH恰好完全反应生成醋酸钠,醋酸钠溶液显碱性,故恰好完全反应的点在M点左侧靠近M点。
A.由分析可知,恰好完全反应的点在M点左侧靠近M点处,A错误;
B.由分析可知,碱中c(OH-)=0.1mol/L,醋酸浓度为0.1mol/L,由于醋酸是弱酸,部分电离,醋酸中c(H+)<0.1mol/L,B错误;
C.由分析可知,NaOH溶液的物质的量浓度为![]()
![]() ,C正确;
,C正确;
D.醋酸浓度和NaOH浓度相等,在N点,醋酸溶液体积是NaOH溶液体积的2倍,故N点,溶质为等物质的量的CH3COONa和CH3COOH,CH3COONa和CH3COOH都能电离产生CH3COO-,故c(CH3COO-)最大。CH3COONa是强电解质,全部电离产生醋酸根离子和钠离子,CH3COOH是弱电解质,部分电离产生醋酸根离子和氢离子,故c(Na+)>c(CH3COOH)>c(H+),综上所述,c(CH3COO-)>c(Na+)>c(CH3COOH) >c(H+),D错误。
答案选C。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目