题目内容
【题目】小苏打(NaHCO3)试样中含有碳酸钠晶体(Na2CO3·l0H2O),为测定试样中小苏打的质量分数w(NaHCO3),实验小组同学设计了如下装置进行实验。
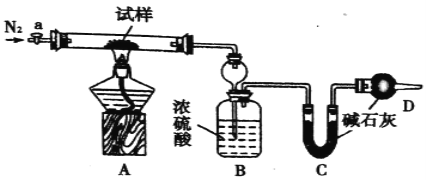
实验过程:
I.按图组装仪器,检查装置的气密性;
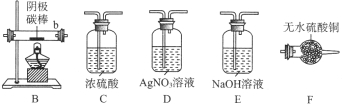
II.将m1 g试样放入硬质玻璃管中,装置B、C、D中药品如图,已知加药品后装置B的质量为m2g、装置C的质量为m3 g;
Ⅲ.关闭活塞a,点燃酒精灯加热试样,直到B装置中无气泡冒出后,打开活塞a向装置中通入N2,一段时间后,撤掉酒精灯,关闭活塞a;
Ⅳ.称得装置B的质量为m4g、装置C的质量为m5g。
请回答以下问题(装置中原有空气对实验的影响忽略不计):
(1)装置A中发生反应的化学方程式为:________________;_______________。
(2)装置B的作用为_______________。装置C的作用为_______________。
(3)实验过程中通入N2的目的为__________。
(4)实验结束后发现装置A中硬质玻璃管右端有水珠,则w(NaHCO3)的计算式为:____________。
【答案】(1)2NaHCO3![]() Na2CO3+CO2+H2O、Na2CO3·10H2O
Na2CO3+CO2+H2O、Na2CO3·10H2O![]() Na2CO3+10H2O
Na2CO3+10H2O
(2)吸收反应生成的水蒸气 (2分)吸收反应生成的CO2;(2分)
(3)把装置中的CO2和水蒸气排出被装置B和装置C完全吸收;(2分)
(4)![]() (3分)
(3分)
【解析】
试题分析:(1)碳酸氢钠和碳酸钠晶体受热均易分解,则装置A中发生反应的化学方程式分别为2NaHCO3![]() Na2CO3+H2O+CO2↑、Na2CO3·10H2O
Na2CO3+H2O+CO2↑、Na2CO3·10H2O![]() Na2CO3+10H2O。
Na2CO3+10H2O。
(2)浓硫酸吸收反应中产生的水蒸气,装置C的作用为吸收反应生成的CO2。
(3)装置有残留的CO2和水蒸气,所以实验过程中通入N2的目的为把装置中CO2和水蒸气排出,被装置B和装置C吸收。
(4)由于只有碳酸氢钠分解产生CO2,所以利用固体的质量和反应中产生的CO2质量即可以计算碳酸氢钠的质量分数,则w(NaHCO3)的计算式为![]() 。
。

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案