��Ŀ����
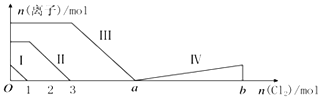
����Ŀ����ҵ�����������Ҫ��Ӧ֮һΪ2SO2(g)+O2(g)![]() 2SO3(g)����Ӧ�����������ı仯��ͼ��ʾ��
2SO3(g)����Ӧ�����������ı仯��ͼ��ʾ��
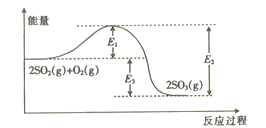
��1����ͼ��֪�÷�Ӧ������ӦΪ_____________(��������������������)��Ӧ��
��2�������¶ȣ�ƽ����_________(��������Ӧ�������淴Ӧ��)�����ƶ�������Ӧ����_____(��������������С����������������ͬ�����淴Ӧ����_____________��
��3����Ӧ��ϵ�м��������ͼ��E1____(��������������С����������������ͬ����E3___________��
��4����֪��2H2S(g)+O2(g)=2S(s)+2H2O(g) ��H=-442.4 kJ��mol-1��
S(s)+O2(g)=SO2(g) ��H=-297.0 kJ mol-1��
��H2S(g)��O2(g)��Ӧ����SO2(g)��H2O(g)���Ȼ�ѧ����ʽ��_________________�����˷�Ӧת��3 mol����ʱ���ų�������Ϊ_______kJ��
���𰸡� ���� �淴Ӧ ���� ���� ��С ���� 2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ��H=-1036.4kJ��mol-1 259.1
��������(1)��Ӧ�з�Ӧ�����������������������������ʷ�ӦΪ���ȷ�Ӧ���ʴ�Ϊ�����ȣ� (2) ���£����ȷ�Ӧ�����ƶ�������Ӧ���淴Ӧ���ʶ����ʴ�Ϊ���淴Ӧ��������������3��������������Խ��ͷ�Ӧ�Ļ��E1������Ӧ��E3���䣬�ʴ�Ϊ����С�����䣻��4�����ݸ�˹���ɷ�������2H2S(g)+O2(g)=2S(s)+2H2O(g) ��H=-442.4 kJ��mol-1��
��S(s)+O2(g)=SO2(g) ��H=-297.0 kJ mol-1������+�ڡ�2���ɵ��Ȼ�ѧ����ʽΪ2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ��H=-442.4-297.0��2=-1036.4kJ��mol-1���÷�Ӧ��ת��12Ħ�����ӣ����Ե�ת��3Ħ������ʱ�ų�������Ϊ1036.4/4= 259.1 kJ���ʴ�Ϊ��2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ��H=-1036.4kJ��mol-1 �� 259.1��

 Сѧ��ʱ��ҵȫͨ����ϵ�д�
Сѧ��ʱ��ҵȫͨ����ϵ�д� �����ÿ�ʱѵ��ϵ�д�
�����ÿ�ʱѵ��ϵ�д� ��Ԫȫ��������ϵ�д�
��Ԫȫ��������ϵ�д� �»ƸԱ����ܾ�ϵ�д�
�»ƸԱ����ܾ�ϵ�д�����Ŀ����ν�Ͻ𣬾��Dz�ͬ�ֽ���(Ҳ����һЩ�ǽ���)���ۻ�״̬���γɵ�һ���ۺ���±�Ϊ���ֽ������ۡ��е㣺
Na | Cu | Al | Fe | |
�۵�/�� | 97.5 | 1083 | 660 | 1535 |
�е�/�� | 883 | 2595 | 2200 | 3000 |
�������������ж����в����γɺϽ����(����)
A. Cu��NaB. Fe��Cu
C. Fe��AlD. Al��Na