题目内容
对于反应2S02+02 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”).
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”).
 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”).
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”).| 编号 | 改变的条件 | 生成SO3一的速率 |
| ① | 升高温度 | 增大 增大 |
| ② | 降低温度 | 减小 减小 |
| ③ | 增大氧气的浓度 | 增大 增大 |
| ④ | 使用催化剂 | 增大 增大 |
| ⑤ | 压缩体积 | 增大 增大 |
分析:影响化学反应速率的因素有温度、浓度、压强、催化剂等,从改变外界条件对活化分子的浓度或百分数的影响角度分析化学反应速率的变化.
解答:解:①升高温度,活化分子的百分数增大,反应速率增大,故答案为:增大;
②降低温度,活化分子百分数减小,反应速率减小,故答案为:减小;
③增大氧气的浓度,反应物活化分子浓度增大,反应速率增大,故答案为:增大;
④使用催化剂,降低反应的活化能,活化分子百分数增大,反应速率增大,故答案为:增大;
⑤压缩体积,压强增大,反应物的浓度增大,活化分子浓度增大,反应速率增大,故答案为:增大.
②降低温度,活化分子百分数减小,反应速率减小,故答案为:减小;
③增大氧气的浓度,反应物活化分子浓度增大,反应速率增大,故答案为:增大;
④使用催化剂,降低反应的活化能,活化分子百分数增大,反应速率增大,故答案为:增大;
⑤压缩体积,压强增大,反应物的浓度增大,活化分子浓度增大,反应速率增大,故答案为:增大.
点评:本题考查外界条件对反应速率的影响,题目难度不大,注意外界条件对活化分子的影响,注重基础知识的积累.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
(6分)对于反应2S02+02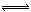 2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
| 编号 | 改变的条件 | 生成SO3的速率 |
| ① | 升高温度 | |
| ② | 降低温度 | |
| ③ | 增大氧气的浓度 | |
| ④ | 使用催化剂 | |
| ⑤ | 压缩体积 | |
| ⑥ | 恒容下充人Ne | |
(6分)对于反应2S02+02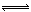 2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
2SO3(g)当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
|
编号 |
改变的条件 |
生成SO3的速率 |
|
① |
升高温度 |
|
|
② |
降低温度 |
|
|
③ |
增大氧气的浓度 |
|
|
④ |
使用催化剂 |
|
|
⑤ |
压缩体积 |
|
|
⑥ |
恒容下充人Ne |
|
(12分)(1)某温度时,在4 L容器中X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为 。
反应开始至2min,Z的平均反应速率为 。若X、Y、Z均为气体,反应达平衡时:此时体系的压强是开始时的 倍。
(2)对于反应2S02+02![]() 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
编号 | 改变的条件 | 生成SO3的速率 |
① | 升高温度 |
|
② | 降低温度 |
|
③ | 增大氧气的浓度 |
|
④ | 使用催化剂(正) |
|
⑤ | 压缩体积 |
|
⑥ | 减少S02的浓度 |
|
 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”).
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成的S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”).