题目内容
(12分)(1)某温度时,在4 L容器中X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式为 。
反应开始至2min,Z的平均反应速率为 。若X、Y、Z均为气体,反应达平衡时:此时体系的压强是开始时的 倍。
(2)对于反应2S02+02![]() 2SO3(g),当其他条件不变时,只改变一个反应条件,将生成S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
2SO3(g),当其他条件不变时,只改变一个反应条件,将生成S03的反应速率的变化填入下表空格内(填“增大”、“减小”或“不变”)。
编号 | 改变的条件 | 生成SO3的速率 |
① | 升高温度 |
|
② | 降低温度 |
|
③ | 增大氧气的浓度 |
|
④ | 使用催化剂(正) |
|
⑤ | 压缩体积 |
|
⑥ | 减少S02的浓度 |
|
(1) 3 X + Y ![]() 2 Z 。0.025 mol /(L?min)。0.9倍。
2 Z 。0.025 mol /(L?min)。0.9倍。
(2)
编号 | 改变的条件 | 生成SO3的速率 |
① | 升高温度 | 增大 |
② | 降低温度 | 减小 |
③ | 增大氧气的浓度 | 增大 |
④ | 使用催化剂(正) | 增大 |
⑤ | 压缩体积 | 增大 |
⑥ | 减少S02的浓度 | 减小 |

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案 新黄冈兵法密卷系列答案
新黄冈兵法密卷系列答案(12分) 恒容密闭容器中,某化学反应2A B+D在四种不同条件下进行,B、D起始浓度为0,反应物A的浓度(mol/L)随反应时间(min)的变化情况如下表:
| 实验序号 | 浓度(mol/L) | 时间(min) | |||||||
| 0 | 10 | 20 | 30 | 40 | 50 | 60 | |||
| 1 | 温 度 | 8000C | 1.0 | 0.80 | O.64 | 0.57 | 0.50 | 0.50 | 0.50 |
| 2 | 8000C | C2 | 0.60 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 | |
| 3 | 8000C | C3 | 0.92 | 0.75 | 0.63 | 0.60 | 0.60 | 0.60 | |
| 4 | 8200C | 1.0 | 0.40 | 0.25 | 0.20 | 0.20 | 0.20 | 0.20 |
根据上述数据,完成下列填空:
(1)在实验1,反应在前20min内用B的浓度变化来表示的平均速率
为 mol/(L·min)。
(2)在实验2,A的初始浓度c2= mol/L,反应在 20分钟内就达到
平衡,可推测实验2中还隐含的条件是 。
(3)设实验3的反应速率为υ3,实验1的反应速率为υ1(用同种物质的浓度变
化表示),则达到平衡时υ3 υ1(填>、=、<=)
且c3 = mol/L。
(4)比较实验4和实验1,可推测该反应是 反应(选填“吸热”、“放热”)。
(5) 800℃时,反应2A B+D的平衡常数= ,
实验2中达到平衡时A的转化率= 。
(12分)氨在国民经济中占有重要的地位,请参与下列探究。
(1)生产氢气:将水蒸气通过红热的炭即产生水煤气。
C(s) + H2O(g) H2(g) + CO(g), ΔH =" +131.3" kJ·mol-1,ΔS =" +133.7" J·mol-1·K-1
H2(g) + CO(g), ΔH =" +131.3" kJ·mol-1,ΔS =" +133.7" J·mol-1·K-1
该反应在低温下能否自发进行 (填:“能”或“否”)。
(2)已知在400℃时,N2 (g)+ 3H2(g) 2NH3(g)的K=0.5,
2NH3(g)的K=0.5,
①2NH3(g) N2 (g)+ 3H2(g)的K= (填数值)。
N2 (g)+ 3H2(g)的K= (填数值)。
②400℃时,在0.5L的反应容器中进行合成氨反应,一段时间后,测得N2、H2、NH3的物质的量分别为2mol、1mol、2mol,则此时反应v(N2)正 v(N2)逆(填:>、<、=、不能确定)
(3)在三个相同容器中各充入1 molN2和3molH2,在某一不同条件下反应并达到平衡,氨的体积分数随时间变化曲线如下图。下列说法正确的是 (填字母)。
| A.图Ⅰ可能是不同压强对反应的影响,且P2>P1 |
| B.图Ⅱ可能是不同压强对反应的影响,且P1>P2 |
| C.图Ⅲ可能是不同温度对反应的影响,且T1>T2 |
| D.图Ⅱ可能是同温同压下,催化剂性能,1>2 |
 H2(g)
+ CO(g), ΔH = +131.3 kJ·mol-1,ΔS = +133.7 J·mol-1·K-1
H2(g)
+ CO(g), ΔH = +131.3 kJ·mol-1,ΔS = +133.7 J·mol-1·K-1
 生成,同时观察到还有一种红棕色气体产生,该气体的分子式是
。
生成,同时观察到还有一种红棕色气体产生,该气体的分子式是
。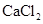 ,
, 溶液 ③加入稀
溶液 ③加入稀 酸化 ④加入NaOH溶液
酸化 ④加入NaOH溶液