题目内容
 某小组利用下列装置进行电化学实验,下列实验操作及预期现象正确的是( )
某小组利用下列装置进行电化学实验,下列实验操作及预期现象正确的是( )分析:A、根据原电池中电子的移动方向知识来回答;
B、原电池的两极金属活泼性相差越大,则化学反应速率越快,电流越大;
C、电解池的阳极是活泼电极,则电极本身失电子发生氧化反应;
D、电解池的阳极是活泼电极,则电极本身失电子发生氧化反应.
B、原电池的两极金属活泼性相差越大,则化学反应速率越快,电流越大;
C、电解池的阳极是活泼电极,则电极本身失电子发生氧化反应;
D、电解池的阳极是活泼电极,则电极本身失电子发生氧化反应.
解答:解:A、X和Y与电流表连接,会构成原电池,电子由负极Zn极流向正极Cu极,故A错误;
B、将Zn换成Fe,则原电池的两极金属活泼性相差不如不换时候大,则化学反应速率会减慢,电流量小,故B错误;
C、X和Y分别与电源“-”、“+”极相连,则Cu做了电解池的阳极,则电极Cu本身失电子发生氧化反应,质量减轻,Zn极析出金属铜质量增加,故C正确;
D、X和Y分别与电源“-”、“+”极相连,则Cu做了电解池的阳极,则电极Cu本身失电子发生氧化反应,质量减轻,Zn极析出金属铜质量增加,故D错误.
故选C.
B、将Zn换成Fe,则原电池的两极金属活泼性相差不如不换时候大,则化学反应速率会减慢,电流量小,故B错误;
C、X和Y分别与电源“-”、“+”极相连,则Cu做了电解池的阳极,则电极Cu本身失电子发生氧化反应,质量减轻,Zn极析出金属铜质量增加,故C正确;
D、X和Y分别与电源“-”、“+”极相连,则Cu做了电解池的阳极,则电极Cu本身失电子发生氧化反应,质量减轻,Zn极析出金属铜质量增加,故D错误.
故选C.
点评:本题考查原电池和电解池,侧重反应原理的考查,考查点较全面细致,注重学生基础知识和基本能力的考查,题目难度不大.

练习册系列答案
相关题目
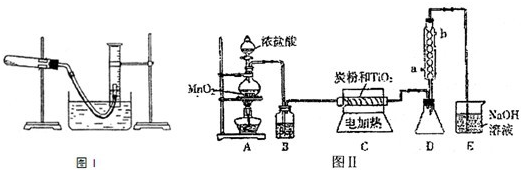
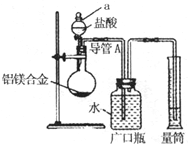 含镁3%~5%的铝镁合金是轮船制造、化工生产、机械制造等行业的重要材料.现有一块质量为m g的铝镁合金,欲测定其中镁的质量分数,几位同学设计了不同的实验方案.
含镁3%~5%的铝镁合金是轮船制造、化工生产、机械制造等行业的重要材料.现有一块质量为m g的铝镁合金,欲测定其中镁的质量分数,几位同学设计了不同的实验方案.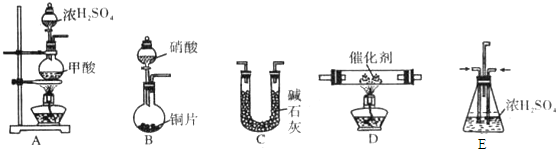
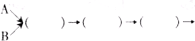 收集气体(填写装置编号)
收集气体(填写装置编号)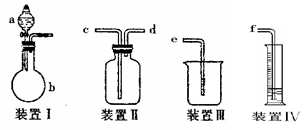

 置序号
置序号