题目内容
【题目】从海水中得到的粗食盐水中常含Ca2+、Mg2+、SO42—,需要分离提纯。现有含少量CaCl2、MgCl2、Na2SO4的粗食盐水,在除去悬浮物和泥沙之后,要用4种试剂:①盐酸、②Na2CO3、③NaOH、④BaCl2来除去食盐水中的Ca2+、Mg2+、SO42—。提纯时的操作步骤和加入试剂的情况如图。
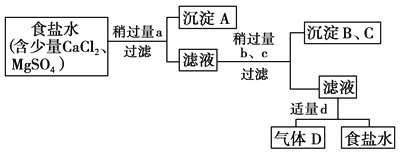
图中a、b、c、d分别表示上述4种试剂中的一种。若a为BaCl2溶液,请回答:
(1)沉淀A的是________。(填化学式)
(2)过滤操作需要的玻璃仪器有___________________________。
(3)试剂d是________;判断试剂d已经过量的方法是:________________________。
(4)加入b、c后溶液中发生的化学反应的化学方程式有:MgCl2 + 2NaOH == Mg(OH)2 ↓ + 2NaCl;
____________________________________________ ;_________________________________。
(5)检验粗食盐水中含有SO42—的方法是___________________________________________________。
【答案】硫酸钡漏斗、玻璃棒、烧杯盐酸溶液中不会再产生气体Na2CO3+CaCl2=CaCO3↓+2NaCl Na2CO3+BaCl2=BaCO3↓+2NaCl用干净的试管取上层清液,向试管中滴加BaCl2溶液,若有沉淀生成说明含有SO42—
【解析】
根据镁离子会与氢氧根离子和碳酸根离子生成沉淀,钙离子会与碳酸根离子生成沉淀,硫酸根离子会与钡离子生成沉淀,加入盐酸可以除去过量的碳酸钠和氢氧化钠。
(1)根据加入的试剂确定沉淀的成分;
(2)根据过滤实验用到的仪器以及常见仪器的名称来回答;
(3)根据盐酸可以和碳酸根离子之间的反应来回答;
(4)根据试剂碳酸钠和氢氧化钠的作用分析发生的反应;
(5)根据SO42—的检验方法分析。
镁离子用氢氧根离子沉淀,加入过量的氢氧化钠可以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都行;钙离子用碳酸根离子沉淀,除钙离子加入碳酸钠转化为沉淀;但是加入的碳酸钠要放在加入的氯化钡之后,这样碳酸钠会除去反应剩余的氯化钡。离子都沉淀了,再进行过滤,最后再加入盐酸除去反应剩余的氢氧根离子和碳酸根离子,
(1)4种试剂①盐酸;②Na2CO3;③NaOH;④BaCl2来除去食盐水中Ca2+、Mg2+、SO42-,加入试剂的顺序是④③②①,氯化钡可以将硫酸根离子沉淀,所以沉淀A是硫酸钡,
故答案为:硫酸钡;
(2)过滤实验用到的仪器:漏斗、玻璃棒、烧杯等,
故答案为:漏斗、玻璃棒、烧杯;
(3)试剂d是盐酸,盐酸可以和碳酸根离子之间反应生成水以及二氧化碳,当不再产生二氧化碳时,证明盐酸已经过量,
故答案为:盐酸;溶液中不会再产生气体;
(4)根据以上分析,a为BaCl2溶液,d是盐酸,则b、c为氢氧化钠溶液或碳酸钠溶液。氢氧化钠能和氯化镁生成氢氧化镁和氯化钠,反应的化学方程式为:2NaOH+MgCl2═Mg(OH)2↓+2NaCl,碳酸钠溶液分别和氯化钙、氯化钡溶液反应为:Na2CO3+CaCl2=CaCO3↓+2NaCl,Na2CO3+BaCl2=BaCO3↓+2NaCl,
故答案为:Na2CO3+CaCl2=CaCO3↓+2NaCl;Na2CO3+BaCl2=BaCO3↓+2NaCl;
(5)检验粗食盐水中含有SO42—的方法是用干净的试管取上层清液,向试管中滴加BaCl2溶液,若有沉淀生成说明含有SO42—,
故答案为:用干净的试管取上层清液,向试管中滴加BaCl2溶液,若有沉淀生成说明含有SO42—。