题目内容
19.某难溶物质X是重要的化工原料,用途广泛.取2.796g物质X与焦炭在隔绝空气条件下加热,所得产物经一系列变化如图所示:
(1)固体甲中金属元素在周期表中的位置为第六周期、IIA族,气体乙的电子式
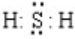 .
.(2)X的化学式是BaSO4.
(3)写出反应①和反应②的化学方程式:①BaSO4+4C$\frac{\underline{\;高温\;}}{\;}$BaS+4CO;②2CO+SO2$\frac{\underline{\;\;△\;\;}}{\;}$S+2CO2.
分析 某难溶物质X与焦炭在隔绝空气条件下加热生成气体甲与固体甲,气体甲与丙反应生成的淡黄色沉淀丁应为S,n(S)=$\frac{0.384g}{32g/mol}$=0.012mol,固体甲中含S元素,盐酸反应生成气体乙为H2S,点燃时H2S燃烧生成气体丙为SO2,溶液乙与碳酸铵反应生成白色沉淀丙可能为BaCO3,n(BaCO3)=$\frac{2.364g}{197g/mol}$=0.012mol,可知X中含Ba、S元素的物质的量为1:1,丙为SO2,则X中含O为$\frac{2.796g-0.384g-0.012mol×137g/mol}{16g/mol}$=0.048mol,可知X中Ba、S、O的原子个数比为1:1:4,即X为BaSO4,以此来解答.
解答 解:某难溶物质X与焦炭在隔绝空气条件下加热生成气体甲与固体甲,气体甲与丙反应生成的淡黄色沉淀丁应为S,n(S)=$\frac{0.384g}{32g/mol}$=0.012mol,固体甲中含S元素,盐酸反应生成气体乙为H2S,点燃时H2S燃烧生成气体丙为SO2,溶液乙与碳酸铵反应生成白色沉淀丙可能为BaCO3,n(BaCO3)=$\frac{2.364g}{197g/mol}$=0.012mol,可知X中含Ba、S元素的物质的量为1:1,丙为SO2,则X中含O为$\frac{2.796g-0.384g-0.012mol×137g/mol}{16g/mol}$=0.048mol,可知X中Ba、S、O的原子个数比为1:1:4,即X为BaSO4,
(1)固体甲中金属元素Ba在周期表中的位置为第六周期、IIA族,气体乙的电子式为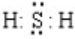 ,
,
故答案为:第六周期、IIA族;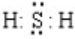 ;
;
(2)X的化学式是BaSO4,故答案为:BaSO4;
(3)反应①和反应②的化学方程式分别为BaSO4+4C$\frac{\underline{\;高温\;}}{\;}$BaS+4CO、2CO+SO2$\frac{\underline{\;\;△\;\;}}{\;}$S+2CO2,故答案为:BaSO4+4C$\frac{\underline{\;高温\;}}{\;}$BaS+4CO;2CO+SO2$\frac{\underline{\;\;△\;\;}}{\;}$S+2CO2.
点评 本题考查无机物的推断,为高频考点,把握转化中发生的反应及淡黄色沉淀为S、白色沉淀丙为碳酸钡为解答的关键,侧重分析与推断能力的考查,题目难度不大.

①4NH3 (g)+5O2 (g)?4NO (g)+6H2O (g)△H=-9072kJ•mol-1?K=1.1×1026?
②4ΝΗ3 (g)+4O2 (g)?2N2O (g)+6H2O (g)△H=-1104.9kJ•mol-1?K=4.4×1028
③4NH3 (g)+3O2 (g)?2N2 (g)+6H2O (g)△H=-1269.02kJ•mol-1?K=7.1×1034
其中,②、③是副反应.若要减少副反应,提高NO的产率,最合理的措施是( )
| A. | 减小压强 | B. | 降低温度 | ||
| C. | 增大O2浓度 | D. | 使用合适的催化剂 |
已知:反应Ⅰ:4NH3(g)+6NO(g)?5N2(g)+6H2O(l)△H1
反应Ⅱ:2NO(g)+O2(g)?2NO2(g)△H2 (且|△H1|=2|△H2|)
反应Ⅲ:4NH3(g)+6NO2(g)?5N2(g)+3O2(g)+6H2O(l)△H3
反应I和反应II在不同温度时的平衡常数及其大小关系如下表
| 温度/K | 反应I | 反应II | 已知: K2>K1>K2′>K1′ |
| 298 | K1 | K2 | |
| 398 | K1′ | K2′ |
(2)相同条件下,反应I在2L密闭容器内,选用不同的催化剂,反应产生N2的量随时间变化如图1所示.
①计算0~4分钟在A催化剂作用下,反应速率v(NO)=0.375mol•L-1•min-1.
②下列说法正确的是CD.
A.该反应的活化能大小顺序是:Ea(A)>Ea(B)>Ea(C)
B.增大压强能使反应速率加快,是因为增加了活化分子百分数
C.单位时间内H-O键与N-H键断裂的数目相等时,说明反应已经达到平衡
D.若在恒容绝热的密闭容器中发生反应,当K值不变时,说明反应已经达到平衡
(3)一定条件下,反应II达到平衡时体系中n(NO):n(O2):n(NO2)=2:1:2.在其它条件不变时,再充入NO2气体,分析NO2体积分数--φ(NO2)的变化情况:(填“变大”、“变小”或“不变”)恒温恒压容器,φ(NO2)不变;恒温恒容容器,φ(NO2)变大.
(4)一定温度下,反应III在容积可变的密闭容器中达到平衡,此时容积为3L,c(N2)与反应时间t变化曲线X如下图所示,若在t1时刻改变一个条件,曲线X变为曲线Y或曲线Z.则:
①变为曲线Y改变的条件是加入催化剂.变为曲线Z改变的条件是将容器的体积快速压缩至2L.
②若t2降低温度,t3达到平衡,请在图2中画出曲线X在t2-t4内 c(N2)的变化曲线.

①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸;②用NaOH溶液除去苯中的少量苯酚;③用饱和NaHCO3溶液除去CO2中的少量SO2;④用加热的方法提取NH4Cl固体中混有的少量碘;⑤用酒精萃取碘水中的碘.
| A. | ①⑤ | B. | ①②④⑤ | C. | ②③ | D. | ②③⑤ |
| A. | 1:2:3 | B. | 1:2:2 | C. | 6:3:2 | D. | 1:1:1 |
| A. | 80% | B. | 60% | C. | 40% | D. | 20% |
| 选项 | 操作方法 | 实验原理 |
| A | 铁粉中混有少量铝粉:溶于浓氢氧化钠溶液,过滤 | 铝粉与氢氧化钠溶液反应,铁粉不和氢氧化钠溶液反应 |
| B | 氯化亚铁溶液中混有氯化铁:加入足量铜粉,过滤 | 铜能将Fe3+还原成Fe2+,铜与Fe2+不反应 |
| C | 过氧化钠中混有氧化钠:在空气中灼烧固体 | 氧化钠与氧气在加热条件下生成过氧化钠 |
| D | 氯化铝溶液中混有氯化镁:加入足量氢氧化铝,过滤 | 氯化镁水解生成盐酸,盐酸与氢氧化铝反应,促进Mg2+完全水解 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 碳的摩尔质量为12g | |
| B. | 22.4L氢气的物质的量是1mol | |
| C. | 0.1 mol•L-1的NaHSO4 溶液中,阳离子的数目之和为0.2NA | |
| D. | 1molNaCl约含6.02×1023个Cl- |