题目内容
【题目】A元素原子的L层比B元素原子的L层少3个电子,B元素原子核外电子数比A元素原子核外电子总数多5个,则A,B两元素形成的化合物可表示为( )
A.BA2
B.BA3
C.A3B2
D.B3A2
【答案】D
【解析】解:A、B两元素原子的L层上有电子,则K层上肯定填满2个,而B原子核外电子总数比A原子核外电子总数多5, 所以A元素的原子的结构示意图为 ![]() ,B元素原子的结构的示意图为
,B元素原子的结构的示意图为 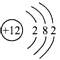 ,
,
即A为氮元素,B为镁元素,形成Mg3N2(氮化镁).
故选D.
A元素原子的L层比B元素原子的L层少3个电子,则A的L层电子应为5,应为N元素,原子核外电子数为7,B元素原子核外电子数比A元素原子核外电子总数多5个,则B的原子核外电子数应为12,为Mg元素,以此解答该题.

练习册系列答案
相关题目
【题目】将0.2mol·L-1的KI溶液和0.05mol·L-1Fe2(SO4)3溶液等体积混合充分反应后,取混合液分别完成下列实验,能说明溶液中存在化学平衡2Fe3++2I-![]() 2Fe2++I2的是
2Fe2++I2的是
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
A.①和③ B.②和④ C.③和④ D.①和②