题目内容
Q、R、T、X、Y、Z是六种原子序数依次增大的前四周期常见元素,其相关信息如下表:
(1)Z元素的原子基态时的电子排布式是________。
(2)下列叙述正确的是________(填字母序号)。
a.Q的气态氢化物比R的气态氢化物稳定
b.Q的含氧酸一定比R的含氧酸酸性强
c.R的气态氢化物的熔点在同族元素的氢化物中最低
d.R的第一电离能、电负性都比Q的大
(3)Q和T可形成两种常见化合物,分别表示为QT和QT2。QT分子中σ键和π键的个数比为________;QT2分子中,Q原子采取________杂化。
(4)笑气(R2T)是一种麻醉剂,有关理论认为R2T与QT2分子具有相似的结构。故R2T的空间构型是________,其为________(填“极性”或“非极性”)分子。
(5)含有Q、Y和镁三种元素的某种晶体具有超导性,其结构如图所示。则该晶体的化学式为________;晶体中每个镁原子周围距离相等且最近的Y原子有______个。

| 元素 | 相关信息 |
| Q | Q的单质是实验室常用的惰性电极材料 |
| R | R原子基态时2p原子轨道上有3个未成对电子 |
| T | 负二价的元素T的氢化物在通常状况下是一种液体,且其中T的质量分数为88.9% |
| X | X是第三周期电负性最大的元素 |
| Y | 元素Y位于周期表的第10列 |
| Z | Z存在质量数为65,中子数为36的核素 |
(1)Z元素的原子基态时的电子排布式是________。
(2)下列叙述正确的是________(填字母序号)。
a.Q的气态氢化物比R的气态氢化物稳定
b.Q的含氧酸一定比R的含氧酸酸性强
c.R的气态氢化物的熔点在同族元素的氢化物中最低
d.R的第一电离能、电负性都比Q的大
(3)Q和T可形成两种常见化合物,分别表示为QT和QT2。QT分子中σ键和π键的个数比为________;QT2分子中,Q原子采取________杂化。
(4)笑气(R2T)是一种麻醉剂,有关理论认为R2T与QT2分子具有相似的结构。故R2T的空间构型是________,其为________(填“极性”或“非极性”)分子。
(5)含有Q、Y和镁三种元素的某种晶体具有超导性,其结构如图所示。则该晶体的化学式为________;晶体中每个镁原子周围距离相等且最近的Y原子有______个。

(1)1s22s22p63s23p63d104s1(或[Ar]3d104s1)
(2)d (3)1∶2 sp (4)直线形 非极性
(5)MgNi3C 12
(2)d (3)1∶2 sp (4)直线形 非极性
(5)MgNi3C 12
Q的单质是实验室常用的惰性电极材料,则Q是C元素;R原子基态时2p原子轨道上有3个未成对电子,故R为N元素;根据氢化物的化学式H2T知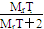 ×100 %=88.9 %,则Mr(T)=16,T为O元素;X是第三周期电负性最大的元素,故X为Cl元素;Y为第四周期第10列的元素,故Y为Ni元素;Z存在质量数为65,中子数为36的核素,因此Z的原子序数为29,故其为Cu元素。(1)Cu元素的原子基态时的电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1。(2)Q的气态氢化物CH4比R的气态氢化物NH3的稳定性差;Q的最高价含氧酸比R的最高价含氧酸酸性弱;R的气态氢化物NH3分子间存在氢键,熔点较高,其熔点在同族元素的氢化物中不是最低的。(3)依据等电子体原理知,CO与N2结构相似,其σ键和π键的个数比为1∶2。(4)N2O和CO2互为等电子体,则N2O的空间构型为直线形,N2O为非极性分子。(5)由结构图可知,C、Ni和镁三种元素的原子个数比为1∶3∶1,晶体中每个镁原子周围距离相等且最近的Y原子有12个。
×100 %=88.9 %,则Mr(T)=16,T为O元素;X是第三周期电负性最大的元素,故X为Cl元素;Y为第四周期第10列的元素,故Y为Ni元素;Z存在质量数为65,中子数为36的核素,因此Z的原子序数为29,故其为Cu元素。(1)Cu元素的原子基态时的电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1。(2)Q的气态氢化物CH4比R的气态氢化物NH3的稳定性差;Q的最高价含氧酸比R的最高价含氧酸酸性弱;R的气态氢化物NH3分子间存在氢键,熔点较高,其熔点在同族元素的氢化物中不是最低的。(3)依据等电子体原理知,CO与N2结构相似,其σ键和π键的个数比为1∶2。(4)N2O和CO2互为等电子体,则N2O的空间构型为直线形,N2O为非极性分子。(5)由结构图可知,C、Ni和镁三种元素的原子个数比为1∶3∶1,晶体中每个镁原子周围距离相等且最近的Y原子有12个。
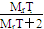 ×100 %=88.9 %,则Mr(T)=16,T为O元素;X是第三周期电负性最大的元素,故X为Cl元素;Y为第四周期第10列的元素,故Y为Ni元素;Z存在质量数为65,中子数为36的核素,因此Z的原子序数为29,故其为Cu元素。(1)Cu元素的原子基态时的电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1。(2)Q的气态氢化物CH4比R的气态氢化物NH3的稳定性差;Q的最高价含氧酸比R的最高价含氧酸酸性弱;R的气态氢化物NH3分子间存在氢键,熔点较高,其熔点在同族元素的氢化物中不是最低的。(3)依据等电子体原理知,CO与N2结构相似,其σ键和π键的个数比为1∶2。(4)N2O和CO2互为等电子体,则N2O的空间构型为直线形,N2O为非极性分子。(5)由结构图可知,C、Ni和镁三种元素的原子个数比为1∶3∶1,晶体中每个镁原子周围距离相等且最近的Y原子有12个。
×100 %=88.9 %,则Mr(T)=16,T为O元素;X是第三周期电负性最大的元素,故X为Cl元素;Y为第四周期第10列的元素,故Y为Ni元素;Z存在质量数为65,中子数为36的核素,因此Z的原子序数为29,故其为Cu元素。(1)Cu元素的原子基态时的电子排布式为1s22s22p63s23p63d104s1或[Ar]3d104s1。(2)Q的气态氢化物CH4比R的气态氢化物NH3的稳定性差;Q的最高价含氧酸比R的最高价含氧酸酸性弱;R的气态氢化物NH3分子间存在氢键,熔点较高,其熔点在同族元素的氢化物中不是最低的。(3)依据等电子体原理知,CO与N2结构相似,其σ键和π键的个数比为1∶2。(4)N2O和CO2互为等电子体,则N2O的空间构型为直线形,N2O为非极性分子。(5)由结构图可知,C、Ni和镁三种元素的原子个数比为1∶3∶1,晶体中每个镁原子周围距离相等且最近的Y原子有12个。
练习册系列答案
相关题目

 的空间构型为 (用文字描述)。
的空间构型为 (用文字描述)。





 、—CH3(甲基)、C
、—CH3(甲基)、C 都是重要的有机反应中间体,有关它们的说法中正确的是( )
都是重要的有机反应中间体,有关它们的说法中正确的是( )