题目内容
碱式碳酸铜可表示为:xCuCO3·yCu(OH)2·zH2O,测定碱式碳酸铜组成的方法有多种。(1)现采用氢气还原法,请回答如下问题:
①写出xCuCO3·yCu(OH)2·zH2O与氢气反应的化学方程式______________________;
②实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
(a)→( )( )→( )( )→( )( )→( )( )→( )( )→(l)
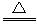
③称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和7.2 g水。该样品的结晶水质量为___________g,化学式为___________________;
(2)某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?请说明理由。
(1)①xCuCO3·yCu(OH)2·zH2O+(x+y)H2![]() (x+y)Cu+xCO2+(x+2y+z)H2O
(x+y)Cu+xCO2+(x+2y+z)H2O
②(a)→kj→gf(或hi)→de(或ed)→hi(或gh)→bc(或cb)→(l)
③1.8 CuCO3·Cu(OH)2·H2O
(2)可行。用氮气代替氢气,氮气可排除空气中CO2、H2O对该实验的影响,xCuCO3·yCu(OH)2·zH2O受热分解为CuO、CO2、H2O,可通过测定CuO、CO2及H2O的质量,进而确定碱式碳酸铜的组成。
解析:本题考查化学方程式的书写、化学计算及实验设计能力。(1)①用H2作还原剂,可使CuCO3、Cu(OH)2被还原为Cu,据电子守恒或原子守恒即可写出反应的化学方程式。②装置连接中,要先对H2进行除杂和干燥,用H2O吸收HCl,再用浓硫酸吸收水蒸气;干燥、纯净的H2与碱式碳酸铜发生反应,生成的H2O和CO2分别用浓硫酸和碱石灰吸收,以便确定H2O和CO2的质量。③由以上分析可知,反应生成的Cu的质量为12.7 g,m(CO2)=4.4 g,则![]() ;由CuCO3被还原生成的Cu的质量为0.1 mol×63.5 g·mol-1=6.35 g,则由Cu(OH)2被还原生成的Cu的质量为12.7 g-6.35 g=6.35 g,Cu(OH)2的物质的量为0.1 mol,所以样品中结晶水质量为:23.9 g-0.1 mol×123.5 g·mol-1-0.1 mol×97.5 g·mol-1=1.8 g,CuCO3、Cu(OH)2、H2O的物质的量之比为:0.1 mol∶0.1 mol∶0.1 mol=1∶1∶1,
;由CuCO3被还原生成的Cu的质量为0.1 mol×63.5 g·mol-1=6.35 g,则由Cu(OH)2被还原生成的Cu的质量为12.7 g-6.35 g=6.35 g,Cu(OH)2的物质的量为0.1 mol,所以样品中结晶水质量为:23.9 g-0.1 mol×123.5 g·mol-1-0.1 mol×97.5 g·mol-1=1.8 g,CuCO3、Cu(OH)2、H2O的物质的量之比为:0.1 mol∶0.1 mol∶0.1 mol=1∶1∶1,
所以碱式碳酸铜的化学式为CuCO3·Cu(OH)2·H2O。
(2)用N2代替H2,N2可排除空气中CO2和H2O对该实验的影响,碱式碳酸铜受热分解为CuO、CO2、H2O,通过测定它们的质量,同样可确定其组成。

碱式碳酸铜可表示为:xCuCO3·yCu(OH) 2·zH2O,测定碱式碳酸铜组成的方法有多种。
![]() (1)现采用氢气还原法,请回答如下问题:
(1)现采用氢气还原法,请回答如下问题:![]()
![]()
![]()
![]()
![]() ①写出xCuCO3·yCu(OH) 2·zH2O与氢气反应的化学方程式 ;
①写出xCuCO3·yCu(OH) 2·zH2O与氢气反应的化学方程式 ;
![]() ②试验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
②试验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
![]() (a)→( )( )→( )( )→( )( )→( )( )→( )( )→(l)
(a)→( )( )→( )( )→( )( )→( )( )→( )( )→(l)
 |
![]()
![]()
![]()
![]()
![]() ③称取23.9g某碱式碳酸铜样品,充分反应后得到12.7g残留物,生成4.4g二氧化碳和7.2g水。该样品的结晶水质量为 g,化学式为 ;
③称取23.9g某碱式碳酸铜样品,充分反应后得到12.7g残留物,生成4.4g二氧化碳和7.2g水。该样品的结晶水质量为 g,化学式为 ;
![]() (2)某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?请说明理由。 。
(2)某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?请说明理由。 。


 (1)现采用氢气还原法,请回答如下问题:
(1)现采用氢气还原法,请回答如下问题: