题目内容
【题目】将4.0 g NaOH和5.3 g Na2CO3混合并配成溶液,向溶液中逐滴缓慢滴加0.5 mol/L稀盐酸。下列图象能正确表示加入盐酸的体积和生成CO2的体积(标况下)的关系的是
A. 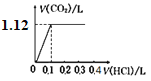 B.
B. 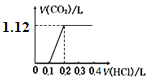
C. 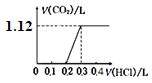 D.
D. 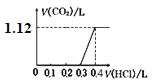
【答案】D
【解析】
将4.0 g NaOH和5.3 g Na2CO3混合并配成溶液,二者的物质的量分别是4.0g÷40g/mol=0.1mol、5.3g÷106g/mol=0.05mol,向溶液中滴加0.5 mol/L稀盐酸,盐酸先与NaOH反应,此时要消耗0.1molHCl,然后发生反应HCl+Na2CO3=NaHCO3+NaCl,又需要消耗HCl0.05mol,都没有二氧化碳气体产生,此时用去的盐酸体积为0.15mol÷0.5 mol/L=0.3L。最后发生反应NaHCO3+HCl=NaCl+H2O+CO2↑,再用去0.05molHCl,产生二氧化碳的物质的量为0.05mol,标准状况下二氧化碳的体积为0.05mol×22.4L/mol=1.12L。答案选D。

 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【题目】观察下列模型并结合有关信息,判断有关说法正确的是( )
B12结构单元 | SF6分子 | S8 | HCN | |
结构模 型示意 图 |
|
|
|
|
备注 | 熔点1873K | — | 易溶于CS2 | — |
A. 单质硼属于原子晶体 B. SF6是由极性键构成的极性分子
C. 固态硫S8属于原子晶体 D. HCN的结构式为HC=N
【题目】已知部分弱酸的电离平衡常数如下表:
弱酸 | HCOOH | HCN | H2CO3 |
电离平衡常数(25℃) | K=1.77×10-4 | K=5.0×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
下列叙述错误的是
A. NaCN溶液中通人少量CO2发生的离子反应为:CN-+H2O+CO2=HCN+HCO3-
B. 等体积、等物质的量浓度的HCOONa和NaCN溶液中所含阴离子总数前者大于后者
C. 等物质的量浓度的NaHCO3和Na2CO3混合溶液中:c(Na+)>c(OH-)>c(HCO3-)>c(CO32-)>c(H+)
D. 中和等体积、等pH的HCOOH溶液和HCN溶液消耗NaOH的物质的量前者小于后者


