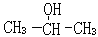题目内容
某有机化合物A的相对分子质量(分子量)大于110,小于150。经分析得知,其中碳和氢的质量分数之和为52.24%,其余为氧。请完成下列问题:(1)该化合物分子中含有几个氧原子,为什么?
(2)该化合物的相对分子质量(分子量)是________。
(3)该化合物的化学式(分子式)是________。
(4)该化合物分子中最多含________个![]() 官能团。
官能团。
解析:由题意知:110<Mr(A)<150,而含氧的质量分数为1-52.24%=47.76%,则分子中氧原子的相对原子质量之和介于110×47.76%—150×47.76%之间,即分子中含氧的相对原子质量之和在52.5—71.6之间,只有4个氧原子(64)时符合题意。所以Mr(A)=![]() =134。设分子中含碳原子x个,氢原子y个,则:CxHyO4 12x+y+64=134 12x+y=70,当x=5,y=10,成立,故A的分子式为C5H10O4,又因为N(C):N(H)=1:2,则分子中只能含有一个
=134。设分子中含碳原子x个,氢原子y个,则:CxHyO4 12x+y+64=134 12x+y=70,当x=5,y=10,成立,故A的分子式为C5H10O4,又因为N(C):N(H)=1:2,则分子中只能含有一个![]() 官能团,其余O原子可以是—OH形式连在其他碳原子上。
官能团,其余O原子可以是—OH形式连在其他碳原子上。
答案:(1)4个氧原子,因为110<Mr (A)<150,且110×47.76%<M(O)总<150×47.76%,即52.5<M(O)总<![]() =4
=4
(2)134 (3)C5H10O4 (4)1

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案
相关题目
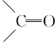 官能团.
官能团.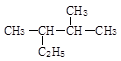 ______________ _
______________ _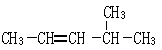 __________________ _
__________________ _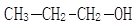 2-丙醇:
2-丙醇: