题目内容
【题目】氯酸镁Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:

已知:
①.卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
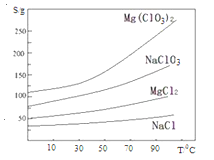
②.四种化合物的溶解度(S)随温度(T)变化曲线如图所示。回答下列问题:
(1).过滤时主要的玻璃仪器有
(2).加入BaCl2的目的是除去杂质离子,检验已沉淀完全的方法是
(3).加入H2O2溶液的作用是: ;加入MgO的作用是
(4).滤渣的主要成分为 。
(5).向滤液中加入NaClO3饱和溶液后,发生反应的化学方程式为:MgCl2 + 2NaClO3 = Mg(ClO3)2↓ + 2NaCl,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为① ;②趁热过滤;③ ;④过滤、洗涤、干燥。
(6).产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.50 g产品配成100 mL溶液。
步骤2: 取10.00 mL于锥形瓶中,加入10.00 mL稀硫酸和20.00mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.l000 mol·L-1K2Cr2O7溶液滴定剩余的Fe2+至终点,此过程中反应的离子方程式为:Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ +6Fe3++7H2O。
步骤4:将步骤2、3重复两次,计算得平均消耗K2Cr2O7溶液15.00 mL。
①写出步骤2中发生反应的离子方程式(还原产物为Cl-)
②产品中Mg(ClO3)2·6H2O的质量分数为 【Mg(ClO3)2·6H2O的相对分子质量为299,列出表达式即可)】
【答案】(1)漏斗、烧杯、玻璃棒;
(2)静置,取上层清液适量于试管中,加入BaCl2溶液,若无白色沉淀生成,则SO42-沉淀完全;
(3)使Fe2+氧化,调节溶液的pH,使Fe3+沉淀完全;
(4)BaSO4和Fe(OH)3;(5)蒸发浓缩,冷却结晶;
(6)①ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O;②(11×299)/(12×3.50)% 即 78.3%。
【解析】
试题分析:(1)过滤时用到的主要玻璃仪器有烧杯、玻璃棒、漏斗,答案为:烧杯、玻璃棒、漏斗;(2)加入BaCl2主要是为了除去SO42-,要检验杂质是否除净的方法为:静置,取上层清液适量于试管中,加入BaCl2溶液,若无白色沉淀生成,则SO42-沉淀完全,答案为:静置,取上层清液适量于试管中,加入BaCl2溶液,若无白色沉淀生成,则SO42-沉淀完全;(3)加入过氧化氢的作用是为了将Fe2+氧化,在调节pH除去,所以为了不引入杂质,加入MgO调节pH,答案为:使Fe2+氧化,调节溶液的pH,使Fe3+沉淀完全;(4)滤渣的主要成分有BaSO4和Fe(OH)3,答案为:BaSO4和Fe(OH)3;(5)向滤液中加入NaClO3饱和溶液后,发生反应的化学方程式为:MgCl2+2NaClO3= Mg(ClO3)2↓+2NaCl,进一步制取Mg(ClO3)2·6H2O就需要除去NaCl,操作步骤为:蒸发浓缩、趁热过滤,再冷却结晶,答案为:蒸发浓缩,冷却结晶;(6)①测定Mg(ClO3)2·6H2O含量的原理是用亚铁离子将氯酸根离子还原为氯离子,再用重铬酸钾滴定剩余的亚铁离子,反应的离子方程式分别为:ClO3- + 6Fe2 + + 6H + = 6Fe3 + + Cl- + 3H2O、Cr2O72- + 6Fe2 + + 14H + = 2Cr3 + + 6Fe3 + + 7H2O,答案为:ClO3- + 6Fe2 + + 6H + = 6Fe3 + + Cl- + 3H2O;②10mL产品中ClO3-的物质的量为:1.000mol/L × 0.02L/6-0.1mol/L × 0.015L = 11/120mol, 产品中Mg(ClO3)2·6H2O得含量为:(11 × 299)/(12 × 3.50)% 即 78.3%,答案为:(11 × 299)/(12 × 3.50)% 即 78.3%

【题目】下列物质的分离提纯方法选择不正确的是
A | 除去氯化钠溶液中的泥沙 | 过滤 |
B | 用四氯化碳提取溴水中的溴 | 萃取 |
C | 分离乙酸(沸点 118℃ )与乙酸乙酯(沸点 77℃ ) | 分液 |
D | 从含有少量氯化钠的硝酸钾溶液中提取硝酸钾 | 结晶 |
A. A B. B C. C D. D