题目内容
12.结构片段为…-CH=CH-CH=CH-…的高分子化合物的单体是( )| A. | 乙烯 | B. | 乙炔 | C. | 正丁烯 | D. | 1,3-丁二烯 |
分析 判断高聚物的单体:首先要根据高聚物的结构简式判断高聚物是加聚产物还是缩聚产物,然后根据推断单体的方法作出判断,
加聚产物的单体推断方法:
(1)凡链节的主链上只有两个碳原子(无其它原子)的高聚物,其合成单体必为一种,将两半链闭合即可;
(2)凡链节主链上只有四个碳原子(无其它原子)且链节无双键的高聚物,其单体必为两种,在正中间画线断开,然后将四个半键闭合即可;
(3)凡链节中主碳链为6个碳原子,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换;
该题属于第(1)种情况,据此进行解答.
解答 解:高分子化合物…CH=CH-CH=CH-CH=CH-CH=CH…,其结构简式可以表示为:-[CH=CH]-n,属于加聚产物,根据加聚产物的单体推断方法,凡链节的主链上只有两个碳原子(无其它原子)的高聚物,其合成单体必为一种,将两半键闭合即可得其单体为:CH≡CH,
故选B.
点评 本题考查加聚反应生原理及高分子化合物单体的求算,题目难度不大,明确加聚反应原理及反应产物的单体判断方法是解答的关键.

练习册系列答案
相关题目
2.根据如图信息,下列说法正确的是( )
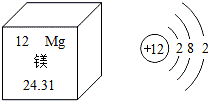

| A. | 镁原子的核电荷数为12 | |
| B. | 镁原子的相对原子质量为24.31g | |
| C. | 镁属于非金属元素 | |
| D. | 在化学反应中,镁原子容易得到电子 |
3.要证明CuSO4溶液显蓝色不是由于SO42-离子造成的,下列实验无意义的是( )
| A. | 观察K2SO4溶液的颜色 | |
| B. | 向CuSO4溶液中滴加适量的NaOH溶液,振荡后静置,溶液颜色消失 | |
| C. | 加水稀释后CuSO4溶液颜色变浅 | |
| D. | 向CuSO4溶液中滴加适量的Ba(NO3)2溶液,振荡后静置,溶液颜色未消失 |
20.金属与不同浓度的硝酸反应时,往往生成多种不同价态的还原产物.图d是各种不同密度的硝酸与铁反应时(相同温度)还原产物的分布图.下列说法不正确的是( )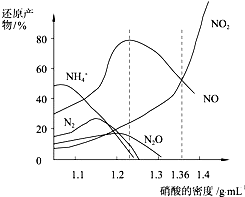

| A. | 密度小于1.1g/mL的硝酸与金属反应,还原产物主要是NH4+ | |
| B. | 当硝酸溶液的密度为1.36g/mL时,Fe与过量硝酸反应的化学方程式为:4Fe+18HNO3=4Fe(NO3)3+3NO+3NO2+9H2O | |
| C. | 稀硝酸与金属反应,一定被还原成NO | |
| D. | 某硝酸试剂瓶的标签注明:密度1.26g/mL,质量分数50.0%;若取该试剂10mL配成1000mL溶液,所得溶液的物质的量浓度为1 mol/L |
17.下列实验过程中涉及的离子反应方程式肯定正确的是( )
| A. | 除去硫酸铜溶液中的硫酸亚铁以最终制备胆矾晶体:2Fe2++Cl2═2Fe3++2Cl- | |
| B. | 含有Mn2+的溶液中加入HNO3酸化,再加入PbO2,反应体系显紫红色:5PbO2+2Mn2++4H+═5Pb2++2MnO4-+2H2O | |
| C. | 向Ba(OH)2溶液中加入过量的NH4HSO4溶液:Ba2++2OH-+NH4++H++SO42-═BaSO4↓+NH3•H2O+H2O | |
| D. | 氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+═Fe3++3H2O |
4.下列有关性质的比较,不能用元素周期律解释的是( )
| A. | 酸性:H2SO4>H3PO4 | B. | 非金属性:O>S | ||
| C. | 碱性:NaOH>Mg(OH)2 | D. | 沸点:HF>HCl |
1.下列说法正确的是( )
| A. | 油脂发生皂化反应能生成甘油 | |
| B. | 蔗糖水解前后均可发生银镜反应 | |
| C. | Fe、Cu、Ag三种金属常用化学还原剂还原法制得 | |
| D. | 向蛋白质溶液中加入CuSO4溶液发生盐析 |
2.下列是几种粒子的结构示意图,有关说法不正确的是( )
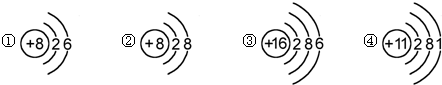

| A. | ①和②属同种元素 | B. | ②属于稀有气体元素 | ||
| C. | ①和③的化学性质相似 | D. | ④属于金属元素 |