题目内容
【题目】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层.科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2 , 化学方程式如下:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g)△H<0
2CO2(g)+N2(g)△H<0
为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(NO) | 1.00×10﹣3 | 4.50×10﹣4 | 2.50×10﹣4 | 1.50×10﹣4 | 1.00×10﹣4 | 1.00×10﹣4 |
c(CO) | 3.60×10﹣3 | 3.05×10﹣3 | 2.85×10﹣3 | 2.75×10﹣3 | 2.70×10﹣3 | 2.70×10﹣3 |
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)前2s内的平均反应速率υ(N2)= , CO的平衡转化率为 . (结果均保留两位有效数字)
(2)写出该反应的平衡常数K的表达式 .
(3)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是 .
A.选用更有效的催化剂
B.升高反应体系的温度
C.降低反应体系的温度
D.缩小容器的体积
(4)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率.某同学设计了三组实验,实验条件已经填在下面实验设计表中.
实验 | T(℃) | NO初始浓度 | CO初始浓度 | 催化剂的比表面积(m2/g) |
Ⅰ | 280 | 1.20×10﹣3 | 5.80×10﹣3 | 82 |
Ⅱ | 280 | 1.20×10﹣3 | 5.80×10﹣3 | 124 |
Ⅲ | 350 | 1.20×10﹣3 | 5.80×10﹣3 | 124 |
①以上三组实验的实验目的是 .
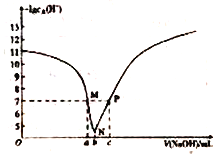
②请在给出的坐标图中,画出上表中的第三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图 . 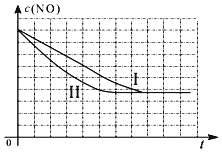
【答案】
(1)1.875×10﹣4mol/(L?s),25%
(2)K= ![]()
(3)C,D
(4)分别验证温度、催化剂比表面积对化学反应速率的影响规律,
【解析】解:(1)前2s内的平均反应速率υ(CO)= ![]() =0.375 mol/(L.s),根据同一段时间内各物质的反应速率之比等于其计量数之比得υ(N2)=
=0.375 mol/(L.s),根据同一段时间内各物质的反应速率之比等于其计量数之比得υ(N2)= ![]() υ(CO)=
υ(CO)= ![]() ×0.375 mol/(L.s)=1.875×10﹣4mol/(Ls),
×0.375 mol/(L.s)=1.875×10﹣4mol/(Ls),
参加反应的c(CO)=(3.60﹣2.70)×10﹣3mol/L,CO转化率= ![]() ×100%=
×100%= ![]() =25%;
=25%;
(2)化学平衡常数K等于生成物浓度幂之积与反应物浓度幂之积的比,则K= ![]() ;
;
(3)A.选用更有效的催化剂只改变化学反应速率,不影响平衡移动,则不能提高CO转化率,故A错误;B.升高反应体系的温度,平衡逆向移动,降低CO转化率,故B错误;
C.降低反应体系的温度,平衡正向移动,提高CO转化率,故C正确;
D.缩小容器的体积,增大压强平衡正向移动,提高CO转化率,故D正确;
(4)①利用控制变量法分析解答,Ⅰ、Ⅱ研究的是催化剂的比表面积对速率的影响,Ⅱ、Ⅲ的催化剂比表面积相同,研究的是温度对速率的影响,Ⅰ、Ⅲ催化剂的比表面积不同,温度不同,研究温度、催化剂的比表面积对反应速率的影响,故目的是:分别验证温度、催化剂比表面积对化学反应速率的影响规律;
②Ⅱ与Ⅰ温度相同,平衡不移动,平衡浓度相同,但Ⅱ催化剂比表面积增大,达平衡时间短,
Ⅲ与Ⅱ的催化剂比表面积相同,Ⅲ温度高,温度升高,不仅达平衡时间缩短,平衡向左移动,使NO的平衡浓度也增大,三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图为:
 ;
;
所以答案是:(1)1.875×10﹣4mol/(Ls);25%;(2)![]() ;(3)CD;(4)①分别验证温度、催化剂比表面积对化学反应速率的影响规律;②
;(3)CD;(4)①分别验证温度、催化剂比表面积对化学反应速率的影响规律;②
【考点精析】本题主要考查了化学平衡的计算的相关知识点,需要掌握反应物转化率=转化浓度÷起始浓度×100%=转化物质的量÷起始物质的量×100%;产品的产率=实际生成产物的物质的量÷理论上可得到产物的物质的量×100%才能正确解答此题.

 阅读快车系列答案
阅读快车系列答案【题目】下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是 ( )
A | B | C | D | |
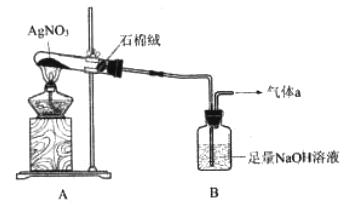
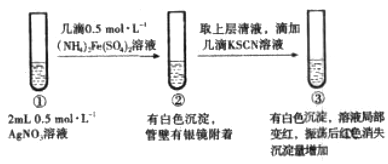
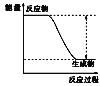
反应 装置或 图像 |
|
|
|
|
实验现 象或图 像信息 | 温度计的 水银柱不 断上升 | 反应物总能 量大于生成 物总能量 | 反应开始后, 甲处液面低 于乙处液面 | 反应开始 后,针筒活 塞向右移动 |
A. A B. B C. C D. D