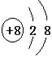
籾朕坪否
a、b、c、d頁膨嶽玉巓豚圷殆。a、b、d揖巓豚⇧c、d揖麼怛。a議圻徨潤更幣吭夕葎 ⇧b嚥c侘撹晒栽麗議窮徨塀葎
⇧b嚥c侘撹晒栽麗議窮徨塀葎 。和双曳熟嶄屎鳩議頁
。和双曳熟嶄屎鳩議頁
 ⇧b嚥c侘撹晒栽麗議窮徨塀葎
⇧b嚥c侘撹晒栽麗議窮徨塀葎 。和双曳熟嶄屎鳩議頁
。和双曳熟嶄屎鳩議頁| A⤴圻徨磯抄⦿a﹅c﹅d﹅b | B⤴窮減來a﹅b﹅d﹅c |
| C⤴圻徨會方⦿a﹅d﹅b﹅c | D⤴恷互勺根剳磨議磨來c﹅d﹅a |
D
喇噐a圻徨宰翌嗤眉蚊窮徨⇧絞葎及眉巓豚圷殆⇧峪嗤x=2憲栽籾吭⇧軸万葎壕圷殆◉序遇辛岑⇧b、d譲葎及眉巓豚圷殆⇧遇b嚥c侘撹晒栽麗議窮徨塀葎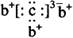 辛容岑b、c蛍艶格孖+1、-3勺⇧夸b葎墜圷殆⇧c葎紀圷殆◉d葎宋圷殆。
辛容岑b、c蛍艶格孖+1、-3勺⇧夸b葎墜圷殆⇧c葎紀圷殆◉d葎宋圷殆。
夸卆象圷殆巓豚舵辛岑⦿
圻徨磯抄⦿b﹅a﹅d﹅c◉窮減來⦿c﹅d﹅a﹅b◉
圻徨會方⦿d﹅a﹅b﹅c◉恷互勺根剳磨議磨來c﹅d﹅a
絞基宛葎D
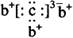 辛容岑b、c蛍艶格孖+1、-3勺⇧夸b葎墜圷殆⇧c葎紀圷殆◉d葎宋圷殆。
辛容岑b、c蛍艶格孖+1、-3勺⇧夸b葎墜圷殆⇧c葎紀圷殆◉d葎宋圷殆。夸卆象圷殆巓豚舵辛岑⦿
圻徨磯抄⦿b﹅a﹅d﹅c◉窮減來⦿c﹅d﹅a﹅b◉
圻徨會方⦿d﹅a﹅b﹅c◉恷互勺根剳磨議磨來c﹅d﹅a
絞基宛葎D

膳楼過狼双基宛
 混邪寄堪選仔表慕芙狼双基宛
混邪寄堪選仔表慕芙狼双基宛
屢購籾朕

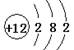 ⇧
⇧