题目内容
【题目】短周期元素X、Y、Z、W在周期表中的相对位置如图所示,其中W元素的原子结构示意图为![]() 。
。
W | X | Y |
Z |
请回答下列问题:
(1)Z元素在元素周期表中的位置是___________。
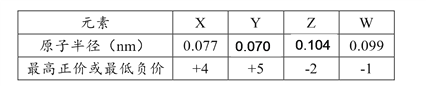
(2)X、Y、Z三种元素的原子半径由大到小的顺序为___________(元素符号表示)。
(3)X、Z、W三种元素的最高价氧化物对应水化物的酸性最强的是___________(用化学式表示)。
(4)用电子式表示WY2的形成过程:___________。
(5)写出W单质与浓硫酸反应的化学方程式:___________。
【答案】第三周期第ⅤA族P>N>OHNO3![]() C+2H2SO4(浓)
C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
【解析】
W元素的原子结构示意图为![]() ,因此b=2,则a=6,所以W是C。根据短周期元素X、Y、Z、W在周期表中的相对位置可知X是N,Y是O,Z是P,据此解答。
,因此b=2,则a=6,所以W是C。根据短周期元素X、Y、Z、W在周期表中的相对位置可知X是N,Y是O,Z是P,据此解答。
根据以上分析可知W是C,X是N,Y是O,Z是P,则
(1)P元素在元素周期表中的位置是第三周期第ⅤA族。
(2)同周期自左向右原子半径逐渐减小,同主族从上到下原子半径逐渐增大,则X、Y、Z三种元素的原子半径由大到小的顺序为P>N>O。
(3)非金属性越强,最高价含氧酸的酸性越强,则X、Z、W三种元素的最高价氧化物对应水化物的酸性最强的是HNO3。
(4)二氧化碳是共价化合物,用电子式表示CO2的形成过程为![]() 。
。
(5)浓硫酸具有强氧化性,与碳反应的化学方程式为C+2H2SO4(浓)![]() CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。

练习册系列答案
相关题目