题目内容
【题目】一定温度下,1 molX和n mol Y在容积为2L的密闭容器中发生如下反应:X(g)+Y(g)![]() 2Z(g)+M(s),5min后达到平衡,此时生成0.2 mol Z。下列说法正确的是
2Z(g)+M(s),5min后达到平衡,此时生成0.2 mol Z。下列说法正确的是
A.若将容器压缩时,正逆反应速率均不变
B.5 min内平均反应速率v(X)=0.02 mol/(L·min)
C.向平衡后的体系中加入l molM(s),平衡向逆反应方向移动
D.当混合气体的质量不再发生变化时,说明反应达到平衡状态
【答案】D
【解析】
试题分析:A.若将容器压缩时,反应物、生成物的浓度都增大,则正逆反应速率都增大,故A错误;B.5 min内生成0.2 mol Z,则消耗0.1 molX,所以X的浓度减小0.1 mol÷2L=0.05mol/L,则用X表示此反应的反应速率是0.05mol/L÷5min=0.01 mol/(L·min),故B错误;C.M是固体,所以M的物质的量增加,对平衡无影响,故C错误;D、当混合气体的质量不再发生变化时,符合化学平衡的特征,说明反应达到平衡状态,故D正确。故选D。

【题目】【2016江苏卷】根据下列实验操作和现象所得到的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 室温下,向苯酚钠溶液中通入足量CO2,溶液变浑浊。 | 碳酸的酸性比苯酚的强 |
B | 室温下,向浓度均为0.1 mol·L–1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀。 | Ksp(BaSO4)<Ksp(CaSO4) |
C | 室温下,向FeCl3溶液中滴加少量KI溶液,再滴加几滴淀粉溶液,溶液变蓝色。 | Fe3+的氧化性比I2的强 |
D | 室温下,用pH试纸测得:0.1mol·L–1 Na2SO3溶液的pH约为10;0.1mol·L–1 NaHSO3溶液的pH约为5。 | HSO3–结合H+的能力比 SO32–的强 |
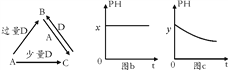
【题目】下表各组物质中,物质之间不可能实现如图![]() 所示转化的是( )
所示转化的是( )
选项 | X | Y | Z | M |
A | Fe(s) | FeCl2 | FeCl3 | Cl2 |
B | NaOH(aq) | Na2CO3 | NaHCO3 | CO2 |
C | NH3(g) | NO | NO2 | O2 |
D | S(s) | SO2 | SO3 | O2 |
A. A B. B C. C D. D