题目内容
化合物A(H3BNH3)是一种潜在的储氢材料,它可由六元环状物质(HB=NH)3通过反应3CH4+2(HB=NH)3+6H2O→3CO2+6H3BNH3制得。有关叙述不正确的是
A.化合物A中存在配位键
B.反应前后碳原子的杂化类型不变
C.CH4、H2O、CO2分子空间构型分别是:正四面体、V形、直线形
D.第一电离能:N>O>C>B
练习册系列答案
相关题目
氮、磷、砷为同主族元素,回答下列问题:
(1)基态As原子的核外电子排布式为___________________。
(2)稼氮砷合金材料的太阳能电池效率达40%,Ga、N、As电负性由大至小的顺序是__________________
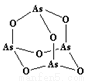
(3)As4O6的分子结构如右图所示,其中As原子的杂化方式为___________________,1 mol As4O6含有σ键的物质的量为_______________。
(4)该族氢化物RH3(NH3、PH3、AsH3)的某种性质随R的核电荷数的变化趋势如右图所示。则Y轴可表示的氢化物(RH3)性质可能是 。

A.稳定性 | B.沸点 | C.R-H键能 | D.分子间作用力 |
(5)AsH3的沸点(-62.5℃)比NH3的沸点(-33.5℃)低,原因是
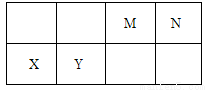
根据下表(部分短周期元素的原子半径及主要化合价)信息,以下判断不正确的是
元素代号 | A | B | C | D | E |
原子半径/nm | 0.186 | 0.143 | 0.089 | 0.102 | 0.074 |
主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
A.金属性:A>C B.氢化物的沸点H2D<H2E
C.第一电离能: A>B D.单质的熔点:A<B


 2PbSO4(s)+2H2O(l)下列说法不正确的是( )
2PbSO4(s)+2H2O(l)下列说法不正确的是( )
 增大
增大 PbSO4(s)+2H2O(l)
PbSO4(s)+2H2O(l)