ƒøƒ⁄»ð
°æƒø°ø‘⁄ µ—È “÷–”√∂˛—ıªØ√Ã∏˙≈®—ŒÀ·∑¥”¶÷∆±∏∏…‘Ô¥ø檵ƒ¬»∆¯°£Ω¯––¥À µ—È£¨À˘”√“«∆˜»ÁÕº£∫
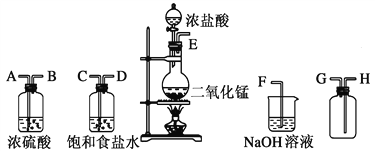
£®1£©¡¨Ω”…œ ˆ“«∆˜µƒ’˝»∑À≥–Ú(ÃÓ∏˜Ω”ø⁄¥¶µƒ◊÷ƒ∏)____________________°£
£®2£©◊∞÷√÷–£¨±•∫Õ ≥—ŒÀƵƒ◊˜”√ «_____________________£ªNaOH»Ð“∫µƒ◊˜”√ «____________°£
£®3£©ªØ—ß µ—È÷–≥£”√ ™»ÛµƒµÌ∑€£≠KI ‘÷ΩºÏ—È «∑Ò”–Cl2≤˙…˙°£»Áπ˚”–Cl2≤˙…˙£¨ø…π€≤ϵΩ________________________£¨∑¥”¶¿Î◊”∑Ω≥Ã ΩŒ™£∫__________________°£
£®4£©–¥≥ˆœ¬¡–ªØ—ß∑¥”¶µƒ∑Ω≥Ã Ω£∫
¢Ÿ∆¯ÃÂ∑¢…˙◊∞÷√Ω¯––µƒ∑¥”¶£∫_________________¢⁄NaOH»Ð“∫÷–∑¢…˙µƒ∑¥”¶£∫____________
£®5£©»ÙΩ´…˙≥…µƒCl2Õ®»ÎµΩ∑÷±÷√”–∏…‘Ô”–…´≤ºÃı∫Õ ™»Û”–…´≤ºÃıµƒ¡Ω∏ˆºØ∆¯∆ø÷–£¨ª·ø¥µΩ ≤√¥œ÷œÛ£∫ _____________________________________°£
°æ¥∞∏°ø E£≠C£¨D£≠A£¨B£≠H£¨G£≠F ≥˝»•¬»∆¯÷–µƒ¬»ªØ«‚∆¯Ã£¨ΩµµÕ¬»∆¯µƒ»ÐΩ‚∂» Œ¸ ’¬»∆¯£¨∑¿÷πø’∆¯Œ€»æ ‘÷Ω±‰¿∂ 2I£≠+Cl2=2Cl£≠+I2 MnO2+4HCl(≈®)![]() MnCl2+Cl2°¸+2H2O 2NaOH+Cl2=NaCl+NaClO+H2O ™»Ûµƒ”–…´≤ºÃıÕ …´£¨∂¯∏…‘Ôµƒ”–…´≤ºÃı≤ªÕ …´
MnCl2+Cl2°¸+2H2O 2NaOH+Cl2=NaCl+NaClO+H2O ™»Ûµƒ”–…´≤ºÃıÕ …´£¨∂¯∏…‘Ôµƒ”–…´≤ºÃı≤ªÕ …´
°æΩ‚Œˆ°ø£®1£©‘⁄ µ—È “÷–”√∂˛—ıªØ√Ã∏˙≈®—ŒÀ·∑¥”¶÷∆±∏∏…‘Ô¥ø檵ƒ¬»∆¯£¨–Ë“™∑¢…˙◊∞÷√…˙≥…¬»∆¯£¨”√±•∫Õ ≥—ŒÀÆ≥˝»•¬»ªØ«‚£¨Õ®π˝≈®¡ÚÀ·≥˝»•ÀÆ’Ù∆¯£¨µº∆¯πÐ≥§Ω¯∂Ã≥ˆ ’ºØ¬»∆¯£¨◊Ó∫Û”√«‚—ıªØƒ∆»Ð“∫Œ¸ ’∂ý”ýµƒ¬»∆¯£¨◊∞÷√¡¨Ω”À≥–Ú «£∫EΩ”C£ªDΩ”A£ªBΩ”H£ªGΩ”F£ª£®2£©±•∫Õ ≥—ŒÀÆ «”√¿¥≥˝»•¬»∆¯÷–µƒ¬»ªØ«‚∆¯Ã£¨ΩµµÕ¬»∆¯µƒ»ÐΩ‚∂»£¨«‚—ıªØƒ∆»Ð“∫Œ¸ ’π˝¡øµƒ¬»∆¯£¨∑¿÷πŒ€»æø’∆¯£ª£®3£©¬»∆¯æþ”–—ıªØ–‘£¨ª·—ıªØµ‚¿Î◊”Œ™µ•÷ µ‚£¨µ‚”ˆµÌ∑€±‰¿∂£¨“Ú¥Àø…π€≤쵽 ‘÷Ω±‰¿∂£¨∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™2I£≠+Cl2=2Cl£≠+I2£ª£®4£©¢Ÿ∑¢…˙◊∞÷√÷– «∂˛—ıªØ√Ã∫Õ≈®—ŒÀ·º”»»∑¥”¶…˙≥…¬»ªØ√𢬻∆¯”ÎÀÆ£¨∑¥”¶∑Ω≥Ã ΩŒ™MnO2+4HCl(≈®)![]() MnCl2+Cl2°¸+2H2O£ª¢⁄¬»∆¯”–∂æ”√«‚—ıªØƒ∆»Ð“∫Œ¸ ’£¨¬»∆¯∫Õ«‚—ıªØƒ∆∑¥”¶…˙≥…¬»ªØƒ∆°¢¥Œ¬»À·ƒ∆∫ÕÀÆ£¨∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™2NaOH+Cl2£ΩNaCl+NaClO+H2O£ª£®5£©∏…‘Ôµƒ¬»∆¯√ª”–∆Ø∞◊–‘£¨¬»∆¯”ÎÀÆ∑¥”¶…˙≥…µƒ¥Œ¬»À·æþ”–«ø—ıªØ–‘£¨“Ú¥À»ÙΩ´…˙≥…µƒCl2Õ®»ÎµΩ∑÷±÷√”–∏…‘Ô”–…´≤ºÃı∫Õ ™»Û”–…´≤ºÃıµƒ¡Ω∏ˆºØ∆¯∆ø÷–£¨ µ—Èœ÷œÛ « ™»Ûµƒ”–…´≤ºÃıÕ …´£¨∂¯∏…‘Ôµƒ”–…´≤ºÃı≤ªÕ …´°£
MnCl2+Cl2°¸+2H2O£ª¢⁄¬»∆¯”–∂æ”√«‚—ıªØƒ∆»Ð“∫Œ¸ ’£¨¬»∆¯∫Õ«‚—ıªØƒ∆∑¥”¶…˙≥…¬»ªØƒ∆°¢¥Œ¬»À·ƒ∆∫ÕÀÆ£¨∑¥”¶µƒªØ—ß∑Ω≥Ã ΩŒ™2NaOH+Cl2£ΩNaCl+NaClO+H2O£ª£®5£©∏…‘Ôµƒ¬»∆¯√ª”–∆Ø∞◊–‘£¨¬»∆¯”ÎÀÆ∑¥”¶…˙≥…µƒ¥Œ¬»À·æþ”–«ø—ıªØ–‘£¨“Ú¥À»ÙΩ´…˙≥…µƒCl2Õ®»ÎµΩ∑÷±÷√”–∏…‘Ô”–…´≤ºÃı∫Õ ™»Û”–…´≤ºÃıµƒ¡Ω∏ˆºØ∆¯∆ø÷–£¨ µ—Èœ÷œÛ « ™»Ûµƒ”–…´≤ºÃıÕ …´£¨∂¯∏…‘Ôµƒ”–…´≤ºÃı≤ªÕ …´°£

 √˚–£øŒÃ√œµ¡–¥∞∏
√˚–£øŒÃ√œµ¡–¥∞∏°æƒø°øœ¬±ÌŒ™‘™Àÿ÷Ð∆⁄±Ìµƒ“ª≤ø∑÷£¨«Î≤Œ’’‘™Àÿ¢Ÿ°´¢ý‘⁄±Ì÷–µƒŒª÷√£¨ªÿ¥œ¬¡–Œ £ª£®ªÿ¥Œ  ±£¨æ˘–Ë π”√‘™Àÿµƒ’Ê µ‘™Àÿ∑˚∫≈£¨≤ªµ√ π”√ ˝◊÷±ý∫≈£©
◊ | ¢ÒA | ¢ÚA | ¢ÛA | ¢ÙA | ¢ıA | ¢ˆA | ¢˜A | ¢¯ |
1 | ¢Ÿ | |||||||
2 | ¢⁄ | ¢€ | ¢Ð | |||||
3 | ¢ð | ¢Þ | ¢þ | ¢ý |
£®1£©¢⁄°¢¢ð°¢¢Þµƒ¬√◊”∞Îæ∂”…¥ÛµΩ–°µƒÀ≥–ÚŒ™
£®2£©–¥≥ˆ”…¢Ÿ°¢¢⁄¡Ω‘™≥∆◊È≥…£¨«“¢Ÿµƒ÷ ¡ø∑÷ ˝◊Ó∏þµƒ∑÷◊”µƒµÁ◊” Ω £¨ –¥≥ˆ∏√ªØ∫œŒÔ∏˙¢ýµƒµ•÷ ∑¢…˙÷√ªª∑¥”¶µƒªØ—ß∑Ω≥Ã Ω £Æ
£®3£©‘™Àÿ¢Þµƒ◊Ó∏þº€—ıªØŒÔø…∫Õ‘™Àÿ¢ðµƒ«‚—ıªØŒÔÀƻГ∫∑¢…˙∑¥”¶£¨–¥≥ˆ∑¥”¶µƒ¿Î◊”∑Ω≥à Ω
£®4£©‘™Àÿ¢€”–∂ý÷÷—ıªØŒÔ£¨∆‰÷–º◊µƒœý∂‘∑÷◊”÷ ¡ø◊Ó–°£ª‘™Àÿ¢Ð”–∂ý÷÷µ•÷ £¨∆‰÷–““µƒœý∂‘∑÷◊”÷ ¡ø◊Ó–°£Æ‘⁄“ª∂®Ãıº˛œ¬£¨Ω´2L º◊∆¯Ã”Î1.5L ““∆¯ÃÂæ˘‘»ªÏ∫œ£¨»Ù∏√ªÏ∫œ∆¯Ã±ª◊„¡øNaOH »Ð“∫ÕÍ»´Œ¸ ’£®√ª”–∆¯ÃÂ≤–¡Ù£©£ÆÀ˘…˙≥…µƒ∫¨—ıÀ·—ŒµƒªØ—ß Ω « £Æ