题目内容
16.德国人弗里茨•哈伯由于发明了合成氨的方法而获得1918年诺贝尔化学奖,他的发明大大提高了农作物的产量同时也提高了硝酸、炸药的产量.下列说法中正确的是( )| A. | N2和H2在点燃或光照条件下可合成氨 | |
| B. | 氨气是弱电解质 | |
| C. | 工业上可使用液氨作制冷剂 | |
| D. | 由氨制取硝酸过程中,氮元素被还原 |
分析 A.氮气和氢气在高温催化剂条件下反应;
B.氨气本身不能电离出自由移动的离子;
C.液氨汽化时吸收大量的热;
D.根据元素的化合价确定元素以及物质发生的化学反应.
解答 解:A.氮气和氢气在点燃或光照条件下不会发生反应,需要在高温催化剂条件下反应生成氨气,故A错误;
B.氨气本身不能电离出自由移动的离子,属于非电解质,故B错误;
C.液氨汽化时吸收大量的热,所以可用作制冷剂,故C正确;
D.由氨制取硝酸过程中,N元素的化合价升高,所以氮元素被氧化了,故D错误;
故选:C.
点评 本题考查了氨气的性质,熟悉氮及其化合物的物理性质和化学性质是解题关键,注意反应条件,题目难度不大.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
7.下列离子组一定能够大量共存的是( )
| A. | CO32-Cl- Na+ H+ | B. | K+ Na+ SO42- Ba2+ | ||
| C. | Cl- Na+ Ag+ NO3- | D. | CO32- SO42- Cl- OH- |
4.下列电离方程式书写错误的是( )
| A. | H2SO4=2H++SO42- | B. | Ba(OH)2=Ba2++2OH- | ||
| C. | Na2CO3=2Na+1+CO3-2 | D. | NaHCO3=Na++HCO3- |
1.有一支25mL酸式滴定管中盛盐酸,液面恰好在amL刻度处,把管内液体放出一部分到bmL刻度线处,盛入量筒内,所得液体体积一定是( )
| A. | (a-b) mL | B. | (25-a)mL | C. | (b-a)mL | D. | 大于a mL |
8.下列化学式能表示一种纯净物的是( )
| A. | C4H10 | B. | C3H6 | C. | C2H6O | D. | CH2Br2 |
5.化学与生活、社会密切相关.下列说法正确的是( )
| A. | 臭氧能对水体消毒,是因为其能杀死水中的病菌 | |
| B. | 执行“限塑令”主要是为了节约资源 | |
| C. | 含磷洗涤剂因为其易被细菌分解,所以不会导致水体污染 | |
| D. | 新装修的住房中放置任何花卉都能降低居室中甲醛的含量 |
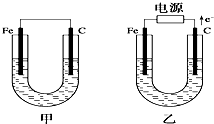 如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题:
如图所示,甲、乙两池电极材料都是铁棒和碳棒,请回答下列问题: