题目内容
实验室需用2 mol·L-1氯化钠溶液450 mL,配置时应选用容量瓶的规格和称取氯化钠的质量分别是
| A.450 mL,52.7g | B.500 mL,58.5g |
| C.1000 mL,117g | D.任意规格,111.2g |
解析试题分析:实验室需用2mol/L氯化钠溶液450mL,只能选用500mL容量瓶配制,实际上配制500mL2mol/L的氯化钠溶液,配制该溶液需要氯化钠的质量为:m(NaCl)=cVM=58.5g/mol×2mol/L×0.5L=58.5g,所以配置时应选用容量瓶的规格和称取氯化钠的质量分别是:500mL、58.5g,故选B.
考点:考查了配制一定物质的量浓度的溶液

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
| |||||||||||||||
| |||||||||||||||
下列有关化学用语使用正确的是
A.钙离子的结构示意图: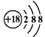 | B.乙烯的结构简式:CH2CH2 |
C.CH4分子的球棍模型: | D.丙烯的电子式: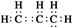 |
由CO2、H2和CO组成的混合气体在同温同压下与氮气的密度相同,则该混合气体中CO2、H2和CO的体积比为 ( )
| A.29:8:13 | B.22:1:14 | C.13:8:29 | D.26:15:57 |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是
A.羟基的电子式为: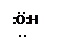 | B.HClO的结构式:H—Cl—O |
C.丙烷分子的比例模型: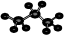 | D.S2-的结构示意图: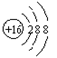 |
在100mL含等物质的量的HBr和H2SO3的溶液里通入0.01mol Cl2,有一半Br-变为Br2(已知Br2能氧化H2SO3)。原溶液中HBr和H2SO3的浓度都等于:
| A.0.0075mol·L-1 | B.0.008mol·L-1 | C.0.075mol·L-1 | D.0.08mol·L-1 |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.0.1molCl2常温下与过量NaOH溶液反应转移电子总数为 0.1NA |
| B.25℃时, pH=13的1.0LBa(OH)2溶液中含有的OH-数目为0.2NA |
| C.0.25mol Na2O2中含有的阴离子数为0.5 NA |
| D.1L0.1mol·L-1的硫化钠溶液中硫离子数目为0.1NA |
某氧化物的相对分子质量为a,其相同价态的硫酸盐的相对分子质量为b,则该元素的化合价的数值为:
| A.(b-a)/20 | B.(b-a)/40 | C.(a -b)/80 | D.(a-b)/20 |