题目内容
某化学课外小组的同学为探究化学反应速率和化学反应限度,做了许多实验,其中两个如下:
实验探究一:温度对化学反应速率的影响
实验步骤:⑴取两个试管,各加入5mL 12%的双氧水(H2O2)溶液
![]() ⑵将其中一支试管直接用酒精灯加热,观察对比两支试管中现象
⑵将其中一支试管直接用酒精灯加热,观察对比两支试管中现象
实验现象:被加热的试管迅速产生大量气泡,未加热的试管缓慢产生气泡
结论:温度越高,反应速率越快。
甲同学认为该实验不够严密,你同意这种看法吗?_________(填“同意”或“不同意”),
原因是_____________________________;如果你认为不够严密,该如何改进?______________________________________________________(认为严密可不填)。
![]() 实验探究二:KI溶液和FeCl3溶液反应(2Fe3+ + 2I- = 2Fe2+ + I2)存在一定的限度。
实验探究二:KI溶液和FeCl3溶液反应(2Fe3+ + 2I- = 2Fe2+ + I2)存在一定的限度。
![]() 可选试剂:①0. 1mol?L -1KI溶液;②0. 1mol?L -1 FeCl3溶液;③FeCl2溶液;④盐酸;⑤KSCN溶液;⑥CCl4。
可选试剂:①0. 1mol?L -1KI溶液;②0. 1mol?L -1 FeCl3溶液;③FeCl2溶液;④盐酸;⑤KSCN溶液;⑥CCl4。
![]() 实验步骤:⑴取5mL 0. 1mol?L -1 KI溶液,再滴加几滴0. 1mol?L -1FeCl3溶液
实验步骤:⑴取5mL 0. 1mol?L -1 KI溶液,再滴加几滴0. 1mol?L -1FeCl3溶液
⑵充分反应后,将溶液分成三份
⑶取其中一份,加试剂____(填序号),用力振荡一段时间,现象_____________,说明___________。
⑷另取一份,加试剂____(填序号),现象___________ ,说明____________。
同意; 一般液体加热沸腾也能观察到大量气泡,不一定是化学反应。改直接加热为水浴加热。⑥;
CCl4层显紫色;说明反应生成碘; ⑤;
显血红色;说明还有Fe3+,反应有一定的限度。

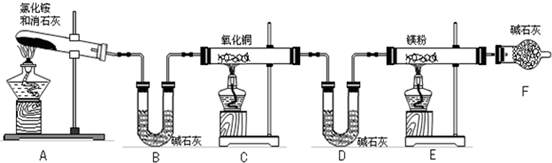
(6分)氨气跟氧化铜反应可以制备氮气,化学方程式:2NH3+3CuO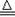 3Cu+3H2O+N2,纯氮气跟镁在高温下反应可得到氮化镁,但氮化镁遇水即剧烈反应生成氢氧化镁和氨气。下面是某化学课外小组的同学提出的实验室制备氨气的几种方案:
3Cu+3H2O+N2,纯氮气跟镁在高温下反应可得到氮化镁,但氮化镁遇水即剧烈反应生成氢氧化镁和氨气。下面是某化学课外小组的同学提出的实验室制备氨气的几种方案:
| A.NH4Cl固体与消石灰(Ca(OH)2)共热 | B.浓氨水逐滴加到新制的生石灰中 |
| C.在一定条件下,N2与H2化合 | D.加热分解NH4Cl固体 |