题目内容
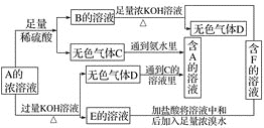
【题目】钛是一种性能非常优越的金属,以钛铁矿(主要成分是FeTiO3,还含有少量Fe2O3)为原料制备钛的流程如下:

(1)FeTiO3中Ti的化合价为_______________________.
(2)步骤①中加Fe的目的是_____________________(用离子方程式表示).
(3)步骤②冷却的目的是______________________________________________.
(4)水浸过程发生的反应为TiO2++2H2O=H2TiO3↓+2H+,从成本或废物的再利用因素考虑,水浸后废液中应加入____________________处理.
(5)写出步骤⑤的化学方程式:____________________________,该反应在Ar气氛中进行的目的是________________________________.
【答案】+4 2Fe3++Fe=3Fe2+ 便于析出FeSO4·7H2O晶体 生石灰(或碳酸钙、废碱,合理即可) ![]() 防止高温下镁(或钛)与空气中的O2、N2反应
防止高温下镁(或钛)与空气中的O2、N2反应
【解析】
钛铁矿的主要成分为FeTiO3,还含有少量Fe2O3,在80℃条件下钛铁矿和浓硫酸混合,发生的反应有FeTiO3+2H2SO4═FeSO4+TiOSO4+2H2O、Fe2O3+3H2SO4═Fe2(SO4)3+3H2O,得到固体熔块,然后用水浸取,浸取液中含有Fe3+,Fe3+能和Fe反应生成Fe2+,然后过滤,滤液冷却,得到硫酸亚铁晶体,TiOSO4能发生水解反应生成H2TiO3和H2SO4,最后高温煅烧H2TiO3得到TiO2,生产TiCl4,TiCl4在800℃和Ar气保护下用Mg还原得到Ti,据此分析解题。
(1)铁为+2价,氧为-2价,由化合价代数和为0得:FeTiO3中Ti的化合价为+4,故答案为:+4;
(2)加铁粉的目的是将溶液里的Fe3+还原为Fe2+,步骤①中加Fe的目的是2Fe3++Fe=3Fe2+(用离子方程式表示),故答案为:2Fe3++Fe=3Fe2+;
(3)根据FeSO4溶解度,从滤液中获得副产品绿矾(FeSO4·7H2O)的具体操作为加热浓缩成饱和溶液,冷却结晶、过滤,少量冰水洗涤、低温干燥,步骤②冷却的目的是便于析出FeSO4·7H2O晶体,故答案为:便于析出FeSO4·7H2O晶体;
(4)水浸过程发生的反应为TiO2++2H2O=H2TiO3↓+2H+,从成本或废物的再利用因素考虑,水浸后废液中应加入生石灰(或碳酸钙、废碱,合理即可)处理,以促进盐的水解,故答案为:生石灰(或碳酸钙、废碱,合理即可);
(5)TiCl4在800℃和Ar气保护下用Mg还原得到Ti,步骤⑤的化学方程式:![]() ,该反应在Ar气氛中进行的目的是防止高温下镁(或钛)与空气中的O2、N2反应,故答案为:
,该反应在Ar气氛中进行的目的是防止高温下镁(或钛)与空气中的O2、N2反应,故答案为:![]() ;防止高温下镁(或钛)与空气中的O2、N2反应。
;防止高温下镁(或钛)与空气中的O2、N2反应。