题目内容
14.只含C、H、O三种元素的有机化合物R的相对分子质量大于110,小于150.经分析得知,其中碳和氢的质量分数之和为52.24%.该化合物分子中最多含( )个碳氧双键.| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
分析 根据含氧量和相对分子质量的范围,得出氧原子数的范围,最终确定分子中含有的氧原子数目,求出有机化合物的相对分子质量,则计算C、H总相对原子质量,利用商余法确定C、H原子数目,进而确定有机物的分子式,结合不饱和度判断.
解答 解:由题意知,氧的质量分数为1-52.24%=47.76%,由有机化合物的相对分子质量大于110,小于150,即分子中氧原子个数为大于$\frac{110×47.76%}{16}$=3.28,小于$\frac{150×47.76%}{16}$=4.48,所以氧原子为4个,氧的质量分数为47.76%,则有机化合物分子质量=$\frac{4×16}{47.76%}$=134,所以C、H的相对原子质量之和为:134-16×4=70,C原子最大数目=$\frac{70}{12}$=5…10,故分子中含有5个C原子、10个H原子,可确定化学式为C5H10O4,与5个C原子的饱和衍生物(可表示为C5H12On)比较可知,不饱和度为1,分子中最多含有1个碳氧双键,
故选A.
点评 本题考查有机物分子式的确定,题目难度中等,计算确定氧原子数为解答该题的关键.

练习册系列答案
 步步高达标卷系列答案
步步高达标卷系列答案
相关题目
4.如图是部分短周期元素化合价与原子序数的关系图,下列说法正确的是( )
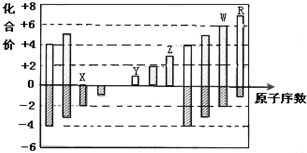

| A. | 原子半径:Z>Y>X | |
| B. | 气态氢化物的稳定性:R>W | |
| C. | 最高价氧化物的水化物的碱性:Y<Z | |
| D. | Y和Z两者最高价氧化物对应的水化物能相互反应 |
5.在某一温度下,某碳氢化合物的蒸气对氢气的相对密度为53.则该化合物的分子式为( )
| A. | C8H10 | B. | CH4 | C. | CH3CH2OH | D. | C5H10 |
2.甲烷分子中4个氢原子被苯基取代,可得如图所示分子,对该分子的描述正确的是( )
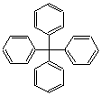

| A. | 此物质属于芳香烃 | B. | 所有碳原子可能在同一平面上 | ||
| C. | 此分子的一氯取代产物有12种 | D. | 此物质分子式为C25H20 |
9.将甲烷与氯气按物质的量之比1:3混合,光照条件下发生化学反应后,得到的有机产物是( )
①CH3Cl ②CH2Cl2 ③CHCl3 ④CCl4.
①CH3Cl ②CH2Cl2 ③CHCl3 ④CCl4.
| A. | 只有① | B. | 只有③ | C. | ①②③的混合物 | D. | ①②③④的混合物 |
19.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 1 mol甲基(-CH3)所含的电子总数为9 NA | |
| B. | 标准状况下,22.4L氯仿所含的共价键为4NA | |
| C. | 常温常压下,142g C10H22中含共价键的数目为31NA | |
| D. | 标准状况下,22.4L甲烷所含的极性共价键数目为4NA |
3.在下列溶液中,各组离子一定能够大量共存的是( )
| A. | 使酚酞试液变红的溶液:Na+、Cl-、SO42-、Fe3+? | |
| B. | 使紫色石蕊试液变红的溶液:Fe2+、Mg2+、NO3-、Cl- | |
| C. | pH=12的溶液:K+、Ba2+、Cl-、Br- | |
| D. | 碳酸氢钠溶液:K+、SO32-、Cl-、H+ |
4.下列关于钠的说法中,正确的是( )
| A. | 钠的化学性质很活泼,所以它在自然界中不能以游离态存在 | |
| B. | 钠可以把钛、锆、铌等金属从它们的氯化物的水溶液中置换出来 | |
| C. | 实验后剩余的钠不可放回原试剂瓶中 | |
| D. | 钠在空气中燃烧生成氧化钠,发出黄色火焰 |