题目内容
12.下列反应最终能生成Fe3+的化合物的是( )①Fe与过量的盐酸反应;②铁丝在硫蒸汽中燃烧;③向FeBr2溶液中通入少量的Cl2;
④铁与CuCl2溶液反应;⑤将Fe(OH)2露置于空气中.
| A. | ①②③ | B. | ①③⑤ | C. | ③④ | D. | ③⑤ |
分析 ①盐酸是非氧化性酸,氧化性比较弱,Fe与HCl反应生成Fe2+;
②铁丝在硫蒸汽中燃烧生成FeS;
③向FeBr2溶液中通入Cl2,Fe2+还原性大于Br-,氯气首先把Fe2+氧化为Fe3+;
④铁与CuCl2溶液反应生成氯化亚铁和铜;
⑤Fe(OH)2露置于空气中,与氧气、水反应生成氢氧化铁.
解答 解:①盐酸是非氧化性酸,氧化性比较弱,只能将铁氧化为亚铁离子,即Fe与HCl反应生成Fe2+,故①不选;
②铁丝在硫蒸汽中燃烧生成FeS,故②不选;
③向FeBr2溶液中通入Cl2,Fe2+还原性大于Br-,氯气首先把Fe2+氧化为Fe3+,故③选;
④铁与CuCl2溶液反应生成氯化亚铁和铜,故④不选;
⑤Fe(OH)2露置于空气中,与氧气、水反应生成氢氧化铁,故⑤选;
故选D.
点评 本题考查了铁及其化合物的性质,难度不大,掌握元素及其化合物的性质是解题的关键,注意氧化剂氧化还原剂时的先后顺序.

练习册系列答案
相关题目
2.如图表示的是向MgCl2、AlCl3的混合溶液中开始时滴加试剂A,之后改滴试剂B,所得沉淀y(mol)与加入试剂体积V(mL)之间的关系.以下结论不正确的是( )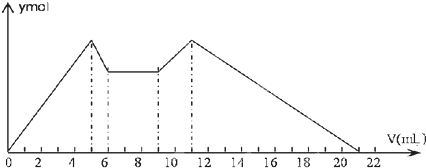

| A. | A是盐酸,B是NaOH溶液,且c(B)=2c(A) | |
| B. | 原混合液中c(Al3+):c(Mg2+):c(Cl-)=1:1:5 | |
| C. | A是NaOH溶液,B是盐酸,且c(NaOH):c(HCl)=2:1 | |
| D. | 从7到9,反应的离子方程式:H++OH-═H2O |
7.对于物质的量相同的硫酸和磷酸(H3PO4),下列说法正确的是( )
| A. | 原子总数相同 | B. | 氧原子数相同 | C. | 质量 | D. | 氢原子数相同 |
17.下列说法或表示方法正确的是( )
| A. | 等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | |
| B. | 由C(s,石墨)=C(s,金刚石)△H=+119 kJ•mol-1可知,石墨比金刚石稳定 | |
| C. | 在稀溶液中:H++OH-═H2O△H=-57.3 kJ•mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ | |
| D. | 在101 kPa时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ•mol-1 |
4.温度为T时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:
下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A. | 反应在前50 s的平均速率为v(PCl3)=0.0032mol•L-1•s-1 | |
| B. | 保持其他条件不变,升高温度,平衡时,c(PCl3)=0.11mol•L-1,则反应的△H<0 | |
| C. | 相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20mol Cl2,达到平衡前v(正)>v(逆) | |
| D. | 相同温度下,起始时向容器中充入2.0 mol PCl3、2.0 mol Cl2,达到平衡时,PCl3的转化率小于80% |
1.将下列各种液体:①苯;②四氯化碳;③碘化钾溶液;④乙烯;⑤植物油,分别与溴水混合后充分振荡、静置,液体分为两层,原溴水层几乎是无色的是( )
| A. | ②⑤ | B. | 只有②④ | C. | ①②④⑤ | D. | ①②③④⑤ |
2.8月12日天津港发生爆炸,专家对爆炸事故原因猜测认为硝化棉或者硫化钠自燃是最可能的点火源,因此化学药品的安全存放是非常重要的.下列有关化学药品的存放说法不正确的是( )
| A. | 液溴易挥发,应用水液封并放在冷暗处保存 | |
| B. | 金属钠遇到氧气立即反应,应保存在煤油中或者液体石蜡里 | |
| C. | 硝酸见光易分解,应用棕色广口试剂瓶保存 | |
| D. | 碳酸钠虽然属于盐,但是其水溶液呈碱性,应用带橡胶塞的试剂瓶保存 |