题目内容
【题目】下列说法正确的是
A. 生成物的总能量大于反应物的总能量时,ΔH<0
B. 在其他条件不变的情况下,使用催化剂可以改变反应的焓变
C. ΔH<0、ΔS >0的反应在低温时不能自发进行
D. 一个化学反应的ΔH只与反应体系的始态和终态有关,而与反应的途径无关
【答案】D
【解析】A、生成物的总能量大于反应物的总能量,此反应是吸热反应,△H>0,故A错误;B、焓变只与始态和终态有关,与反应的途径无关,即使用催化剂不能改变反应的焓变,故B错误;C、根据△G=△H-T△S,因为△H<0,△S>0,因此任何温度下都能自发进行,故C错误;D、根据盖斯定律,故D正确。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
【题目】室温时,两个容积相同的烧瓶中分别盛有M和N两种气体(同温同压)取下弹簧夹A,使两烧瓶内的气体接触(如图),容器内的压强由大到小的顺序是( )
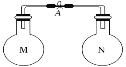
编号 | ① | ② | ③ | ④ |
气体M | HI | NH3 | H2 | NO |
气体N | Cl2 | HCl | N2 | O2 |
A. ①②③④ B. ③①④② C. ④①②③ D. ①④③②