题目内容
在标准状况下15 g CO与CO2的混合气体,体积为11.2 L。则:
(1)混合气体的密度是 。
(2)混合气体的平均摩尔质量是 。
(3)CO2和CO的体积之比是 。
(4)CO的体积分数是 。
(5)CO2和CO的质量之比是 。
(6)CO的质量分数是 。
(7)混合气体中所含氧原子的物质的量是 。
(8)混合气体中所含碳原子的物质的量是 。
(1)1.339 g·L-1
(2)30 g·mol-1
(3)1∶7
(4)87.5%
(5)11∶49
(6)81.7%
(7)0.562 5mol
(8)0.5 mol
【解析】(1)密度= =
=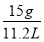 =1.339 g·L-1。
=1.339 g·L-1。
(2)解法一:n=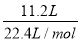 =0.5 mol,M=
=0.5 mol,M=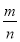 =
=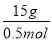 =30 g·mol-1.
=30 g·mol-1.
解法二:M=ρ·Vm=1.339 g·L-1×22.4 L·mol-1=30 g·L-1。
(3)根据阿伏加德罗定律:体积之比=物质的量之比,最简单的方法是用十字交叉法计算:
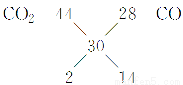
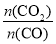 =
=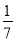 。
。
(4)CO的体积分数=CO的物质的量分数=7÷8×100%=87.5%。
(5) 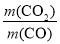 =
=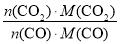 =
=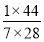 =11∶49
=11∶49
(6)CO的质量分数=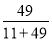 ×100%=81.7%。
×100%=81.7%。
(7)n(O)=2n(CO2)+n(CO)=2×0.5 mol×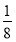 +0.5 mol×
+0.5 mol×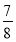 =0.562 5 mol。
=0.562 5 mol。
(8)n(C)=n(CO2)+n(CO)=0.5 mol。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目