题目内容
11.琥珀酸二乙酯是良好的增塑剂和特种润滑剂,也是重要的有机合成的中间体.分析图中物质间的转化关系,回答问题.
已知:RCN$\stackrel{H+}{→}$ RCOOH
(1)B与D的结构简式分别为NCCH2CH2CN、HOCH2CH2OH.
(2)C的同分异构体中,与C具有相同官能团的是CH3CH(COOH)2(写结构简式).
(3)由C制备琥珀酸二乙酯的化学方程式为:HOOC-CH2CH2-COOH+2C2H5OH$→_{△}^{H+}$C2H5OOCCH2CH2COOC2H5+2H2O.
(4)上图转化关系中涉及的基本反应类型有加成反应、取代反应.
(5)若E为高分子化合物,则由C与D制备E的化学方程式为nHO-CH2CH2-OH+nHOOC-CH2CH2-COOH $→_{△}^{H+}$
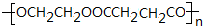 +2nH2O.
+2nH2O.(6)若E为八元环状化合物,其分子式为C6H8O4.
分析 根据题中各物质转化关系,乙烯与溴发生加成反应生成A为BrCH2CH2Br,A在氢氧化钠水溶液、加热条件下发生水解反应生成D为HOCH2CH2OH,A与NaCN发生取代反应生成B为NCCH2CH2CN,B酸性水解得C为HOOCCH2CH2COOH,C在酸、加热条件下与乙醇发生酯化反应琥珀酸二乙酯为CH3CH2OOCCH2CH2COOCH2CH3,HOOCCH2CH2COOH和HOCH2CH2OH,发生酯化反应生成E,E为可为高分子也可为环状化合物,据此答题;
解答 解:根据题中各物质转化关系,乙烯与溴发生加成反应生成A为BrCH2CH2Br,A在氢氧化钠水溶液、加热条件下发生水解反应生成D为HOCH2CH2OH,A与NaCN发生取代反应生成B为NCCH2CH2CN,B酸性水解得C为HOOCCH2CH2COOH,C在酸、加热条件下与乙醇发生酯化反应琥珀酸二乙酯为CH3CH2OOCCH2CH2COOCH2CH3,HOOCCH2CH2COOH和HOCH2CH2OH,发生酯化反应生成E,E为可为高分子也可为环状化合物,
(1)根据上面的分析可知,B为NCCH2CH2CN,D为HOCH2CH2OH,
故答案为:NCCH2CH2CN;HOCH2CH2OH;
(2)C为HOOCCH2CH2COOH,C的同分异构体中,与C具有相同官能团即有两个羧基,其结构的是CH3CH(COOH)2,
故答案为:CH3CH(COOH)2;
(3)C为HOOCCH2CH2COOH,由C制备琥珀酸二乙酯的化学方程式为:HOOC-CH2CH2-COOH+2C2H5OH$→_{△}^{H+}$ C2H5OOCCH2CH2COOC2H5+2H2O,
故答案为:HOOC-CH2CH2-COOH+2C2H5OH$→_{△}^{H+}$ C2H5OOCCH2CH2COOC2H5+2H2O;
(4)根据上面的分析可知,上图转化关系中涉及的基本反应类型有加成反应、取代反应,
故答案为:加成反应、取代反应;
(5)若E为高分子化合物,则由C与D制备E的化学方程式为nHO-CH2CH2-OH+nHOOC-CH2CH2-COOH $→_{△}^{H+}$ 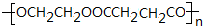 +2nH2O,
+2nH2O,
故答案为:nHO-CH2CH2-OH+nHOOC-CH2CH2-COOH $→_{△}^{H+}$ 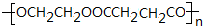 +2nH2O;
+2nH2O;
(6)若E为八元环状化合物,则可由C与D脱去两分子水制得E,所以E的分子式为C6H8O4,
故答案为:C6H8O4.
点评 本题考查有机物的推断,掌握官能团的性质与转化是关键,利用顺推法推断,侧重对基础知识的考查,难度中等.

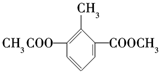
| A. | 一定条件下能发生加成反应和取代反应 | |
| B. | 分子式是C11H12O4 | |
| C. | 苯环上的一氯代物有2种 | |
| D. | 含有一种含氧官能团 |
| A. | 常温下将28 g Fe投人到足量的浓硝酸中,可得到标准状况下33.6 L NO2 | |
| B. | 任何条件下,64 gSO2中含有的原子数目一定为3 NA | |
| C. | 25℃时pH=13的NaOH溶液中含有OH一的数目为0.1 NA | |
| D. | 1 mo1 Na2O2反应生成O2时,必失去2 NA个电子 |
| A. | Na2O2 | B. | Ca( ClO)2 | C. | FeSO4 | D. | 浓盐酸 |
| A. | 16O2与18O2互为同素异形体 | |
| B. | 16O与18O核外电子排布方式不同 | |
| C. | 16O和18O互为同位素 | |
| D. | 1.12L16O2和 1.12L18O2均含有0.1 NA个氧原子 |
| A. | CH2=CH2 | B. | 甲苯 | C. | 苯 | D. | 乙醇 |
| A. | 配制5%NaCl溶液时,将称量的NaCl放入烧杯中加计量的水搅拌溶解 | |
| B. | 配制1mol•L-1NaOH溶液时,将溶解后的NaOH溶液立即注入容量瓶 | |
| C. | 配制0.1mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 | |
| D. | 取用一小块钠时,将剩余的钠丢进废液缸 |