题目内容
【题目】设NA为阿伏加德罗常数的值,下列说法中正确的是
A. 0.2 mol/L CaCl2溶液中含有氯离子的数目为0.4NA
B. 18 g D2O中所含电子数为10NA
C. 2.24 L N2和O2的混合气体中分子数为0.2NA
D. 标准状况下,33.6 L SO3中含有氧原子的数目大于4.5NA
【答案】D
【解析】
A.没有说明溶液的体积,无法计算溶液中氯离子的数目,故A错误;B.物质的量![]() ,D2O中所含电子数= 0.9mol×10×NA=9NA,故B错误;C.没有说明气体所处的温度和压强,无法计算气体中气体的分子的物质的量,故C错误;D.三氧化硫的熔点是16.83℃,在标况下三氧化硫为固体,所以33.6 L SO3的物质的量远大于1.5mol,故含有氧原子的数目大于4.5NA,故D正确;本题选D。
,D2O中所含电子数= 0.9mol×10×NA=9NA,故B错误;C.没有说明气体所处的温度和压强,无法计算气体中气体的分子的物质的量,故C错误;D.三氧化硫的熔点是16.83℃,在标况下三氧化硫为固体,所以33.6 L SO3的物质的量远大于1.5mol,故含有氧原子的数目大于4.5NA,故D正确;本题选D。

练习册系列答案
相关题目
【题目】现有四组分散系:①汽油和水形成的乳浊液;②含有泥沙的食盐水;③溶有碘(I2)的酒精溶液;④乙二醇和丙三醇的混合溶液(乙二醇和丙三醇的部分物理性质见下表)。
物质 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 溶解性 |
乙二醇 | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
丙三醇 | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |
请用下图所示的仪器分离以上各混合液,仪器和方法不能对应的是( )
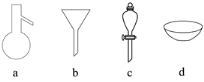
A. ①―c―分液 B. ②―b―过滤 C. ③―d―蒸发结晶 D. ④―a―蒸馏