题目内容
15.辉铜矿石主要含有硫化亚铜(Cu2S)及少量脉石(SiO2).一种以辉铜矿石为原料制备硝酸铜的工艺流程如下: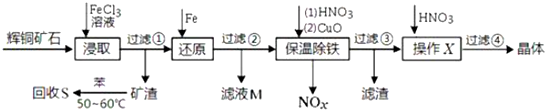
(1)写出步骤“还原”中可能发生反应的离子方程式Fe+2Fe3+═3Fe2+、Fe+Cu2+═Cu+Fe2+.
(2)回收S过程中温度控制50℃~60℃之间,不宜过高的原因是温度高苯容易挥发.
(3)气体NOx与氧气混后通入水中能生成流程中可循环利用的一种物质,该物质的化学式为HNO3;向滤液M中加入(或通入)下列b(填字母)物质,得到另一种可循环利用的物质.
a.铁 b.氯气 c.高锰酸钾 d.盐酸
(4)保温除铁过程中加入CuO的目的是调节溶液的pH,使Fe3+完全转化为Fe(OH)3沉淀;
(5)过滤③所得到的滤液,加入硝酸后,经操作X、过滤④得到硝酸铜晶体.
操作X是蒸发浓缩、冷却结晶(填操作名称).
分析 辉铜矿加入氯化铁溶液溶解浸取过滤,得到矿渣加入苯水浴加热回收硫单质;加入在滤液中加入铁还原铁离子和铜离子过滤,滤液M中加入氯气氧化反应生成氯化铁循环使用,保温除铁加入稀硝酸溶液和氧化铜反应,调节溶液PH除去杂质离子,过滤得到滤液为硫酸亚铁溶液,在稀硝酸溶液中蒸发浓缩,冷却结晶过滤洗涤得到晶体,
(1)铁具有还原性,铁离子、铜离子具有氧化性,均可以与金属铁反应被还原,据此答题;
(2)苯沸点比较低,温度过高苯容易挥发,温度过低溶解速率小;
(3)NOx做还原剂,依据质量守恒和电子守恒写出方程式:4NOx+(5-2x)O2+2H2O=4HNO3,向滤液M中通入Cl2将FeCl2氧化为FeCl3,可以循环使用;
(4)Fe3++3H2O?Fe(OH)3+3H+,加入CuO使水解平衡正向进行,调节溶液的PH使铁元素完全转化为氢氧化铁沉淀;
(5)铜离子属于弱碱阳离子,容易水解呈酸性,加入酸可以抑制其水解,得到晶体的方法是蒸发浓缩溶液,冷却结晶,据此解答即可.
解答 解:(1)铁具有还原性,铁离子、铜离子具有氧化性,均可以与金属铁反应被还原,反应的离子反应方程式分别为:Fe+2Fe3+=3Fe2+、Fe+Cu2+=Cu+Fe2+,
故答案为:Fe+2Fe3+=3Fe2+;Fe+Cu2+=Cu+Fe2+;
(2)苯沸点比较低,温度过高苯容易挥发,温度过低溶解速率小,
故答案为:温度高苯容易挥发;
(3)NOx做还原剂,依据质量守恒和电子守恒写出方程式:4NOx+(5-2x)O2+2H2O=4HNO3,HNO3可以循环使用,向滤液M中通入Cl2将FeCl2氧化为FeCl3,可以循环使用,故选b;
故答案为:HNO3;b;
(4)Fe3++3H2O?Fe(OH)3+3H+,加入CuO使水解平衡正向进行,调节溶液的PH使铁元素完全转化为氢氧化铁沉淀,
故答案为:调节溶液的pH,使Fe3+完全转化为Fe(OH)3沉淀;
(5)铜离子属于弱碱阳离子,容易水解呈酸性,加入酸可以抑制其水解,得到晶体的方法是蒸发浓缩溶液,冷却结晶,
故答案为:蒸发浓缩;冷却结晶.
点评 本题考查了物质分离提纯的方法和流程判断,主要是物质性质的理解应用和实验基本操作,掌握基础是关键,题目难度中等.

 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案| A. | 金属腐蚀就是金属失去电子被还原的过程 | |
| B. | 合金的熔点都高于它的成分金属,合金的耐腐蚀性也都比其成分金属强 | |
| C. | 铜板上的铁铆钉处在潮湿的空气中直接发生反应:Fe-3e-=Fe3+,继而形成铁锈 | |
| D. | 将水库中的水闸(钢板)与外加直流电源的负极相连,正极连接到一块废铁上可防止水闸被腐蚀 |
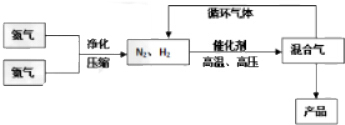
Ⅰ、其部分工艺流程如右图所示,反应体系中各组分的部分性质见下表:
| 气体 | 氮气 | 氢气 | 氨 |
| 熔点(℃) | -210 | -253 | -78 |
| 沸点(℃) | -195 | -259 | -33 |
(1)写出该反应的化学平衡常数表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$.随着温度的升高,K值减小(填增大、减小、不变).平衡常数K值越大,表明AB(填序号).
A.N2的转化率越高 B.NH3的产率越大
C.原料中N2的含量越高 D.化学反应速率越快
(2)合成氨反应的平衡常数很小,所以在工业上采取气体循环的流程.即反应后通过把混合气体的温度降低到-33.42使NH3分离出来;继续循环的气体是N2、H2.
Ⅱ、在一密闭容器中发生该反应,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
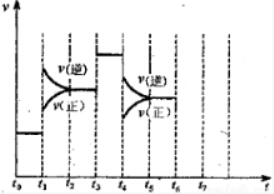
(3)t1、t3、t4时刻分别改变的一个条件是:t1时刻C;t3时刻E;t4时刻B(填选项).
A.增大压强 B.减小压强 C.升高温度
D.降低温度 E.加催化剂 F.充入氮气
(4)依据(2)中的结论,下列时间段中,氨的百分含量最高的是A(填选项).
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6.
| A. | 每生成0.6mol H2,被还原的水分子数目为1.2NA | |
| B. | 有2.7g Al参加反应时,转移的电子数目为0.3NA | |
| C. | 有6.72L H2生成时,反应中转移的电子数目为0.6NA | |
| D. | 溶液中每增加0.1mol AlO${\;}_{2}^{-}$,Na+的数目就增加0.1NA |
| A. | ${\;}_{55}^{131}$I的化学性质与${\;}_{53}^{127}$I是相同 | |
| B. | ${\;}_{53}^{131}$I的原子序数为53 | |
| C. | ${\;}_{53}^{131}$I的原子核外电子数为78 | |
| D. | ${\;}_{53}^{131}$I的原子核内中子数多于质子数 |
| A. | 可以用过滤的方法分离FeCl3溶液和Fe(OH)3胶体 | |
| B. | Fe(OH)3胶体静置会分层 | |
| C. | HCl、SO2、Fe2+均既有氧化性又有还原性 | |
| D. | CH3COONH4的电离方程式为:CH3COONH4 CH3COO-+NH4+ |
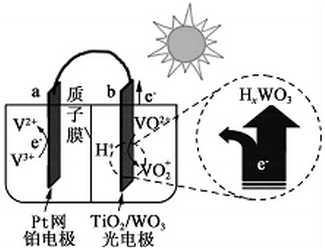
| A. | 该电池与硅太阳能电池供电原理相同 | |
| B. | 光照时,b极周围pH减小 | |
| C. | 光照时,H+由b极室透过质子膜进入a极室 | |
| D. | 夜间无光照时,a为电池的负极 |
| A. | 氯化钠溶液能导电,所以氯化钠溶液是电解质 | |
| B. | NaCl固体不导电,熔融的KCl能导电,所以前者是非电解质,而后者是电解质 | |
| C. | SO2、Na2O的水溶液都能导电,所以它们都是电解质 | |
| D. | 在溶于水或熔融状态下能够自身发生电离的化合物一定是电解质 |
 .
. CH3COO-+NH4++2Ag↓+3NH3+H2O.
CH3COO-+NH4++2Ag↓+3NH3+H2O. .
. .
. .
.