��Ŀ����
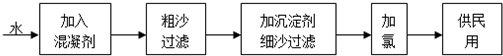
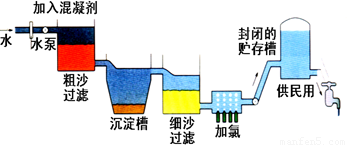
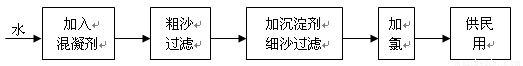
����ˮ����������ʾ��ͼ���£�
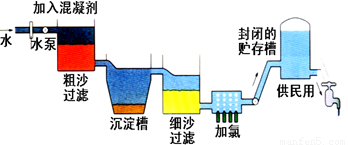
��1����������ȥ�������ʵĹ��� ����д��ţ�
��ֻ�������仯 ��ֻ�ǻ�ѧ�仯 ���������ͻ�ѧ�仯
FeSO4��7H2O�dz��õĻ�����������ˮ���������� ������
��2��ʵ���ҹ��˲������õ��IJ��������� ��
��3��������ʱ�о�����ˮ����Ư����ζ������Ϊʹ����������������д���йصĻ�ѧ��Ӧ����ʽ ��
���������У� ������Ϊ�����Ĵ���Ʒ������д��ţ�
�� ���� ��NH3��Һ�� ��K2FeO4 ��SO2
��4����Щ��������Ȼˮ�к��н϶�ĸơ�þ���ӡ������ӽ�����֬����Ӳˮʱ���Ⱥ��ˮͨ���ֱ�װ�����ӽ�����֬�� ���ӽ�����֬�����ӽ����������������������
��5���ⶨˮ�е��ܽ�������ȡ20mLˮ����Ѹ�ټ���MnSO4��KOH�����Һ���ټ���KI��Һ�������������ӣ���ʹ��ȫ��Ӧ�������ӣ�Ѹ�ټ�������������Һ����ʱ�еⵥ�����ɡ���0.10mol/LNa2S2O3��Һ�ζ����ɵĵ⣬������6.00mL Na2S2O3��Һ����֪�ڼ�����Һ�У�������Ѹ������Mn2+�������������������¿��Խ�����������Ϊ�ⵥ�ʣ��������»�ԭΪMn2+��
�������̷����ķ�Ӧ�ɱ�ʾΪ��2Mn2++4OH��+O2=2MnO(OH)2
MnO(OH)2+2I��+4H+=I2+Mn2++3H2O I2+2S2O32��=2I��+S4O62��
��ˮ�е��ܽ���������mg��g����Ϊ��λ��
��1���ۣ�2�֣� Fe(OH)3��2�֣�
��2��©�� �ձ� ��������3�֣�
��3��Cl2+H2O  HCl+HClO��2�֣��٢ۣ�2�֣��� ��
����2�֣��� 12.0mg��g������2�֣�
HCl+HClO��2�֣��٢ۣ�2�֣��� ��
����2�֣��� 12.0mg��g������2�֣�
��������
�����������1��FeSO4ˮ���Fe(OH)2�� 4 Fe(OH)2 +2 H2O+ O2=4 Fe(OH)3
��3����������������ˮ���ɵ�HClO��������, ������ K2FeO4 ��FeΪ+6�ۣ���ǿ�����ԡ�
��4�����������ӵĽ�����
���㣺�����Թ�������Ϊ��������Ԫ�ؼ��������ѧʵ�������������ѧ��������֪ʶ

 HCl+HClO
K=4.5��10-4
HCl+HClO
K=4.5��10-4