题目内容
【题目】比较下列各项中的前者和后者,用“>”、“<”、或“=”填空
(1)沸点: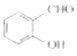
![]()
(2)在水中的溶解度:CH3CH2OHCH3(CH3)2CH2OH
(3)酸性:HClO3HClO4
(4)键长:H-OH-S
(5)未成对电子数:OCr
【答案】(1)<(2)>(3)<(4)<(5)<
【解析】
试题分析:
(1)邻羟基苯甲醛分子内能形成氢键,使沸点降低;对羟基苯甲醛分子间能形成氢键,使沸点升高,则有邻羟基苯甲醛沸点小于对羟基苯甲醛沸点。
(2)羟基为亲水基团,烷基为憎水基团,则烷基所含碳数越多,水溶性越差,故有CH3CH2OH在水中的溶解度大于CH3(CH3)2CH2OH在水中的溶解度。
(3)同一元素所形成的含氧酸,价态越低,酸性越弱,则有HClO3的酸性小于HClO4的酸性。
(4)原子半径越小,共价键键长越短,则有H-O的键长小于H-S的键长。
(5)O的电子排布式为1s22s22p4,含有2个未成对电子。Cr的电子排布式为1s22s22p63s23p63d54s1,含有6个未成对电子。所以未成对电子数:O<Cr。

练习册系列答案
相关题目