题目内容
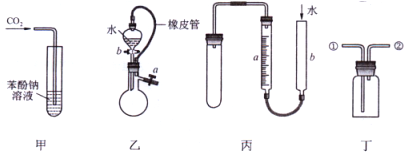
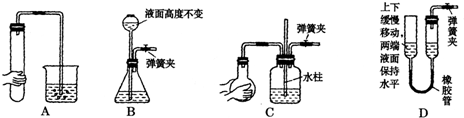
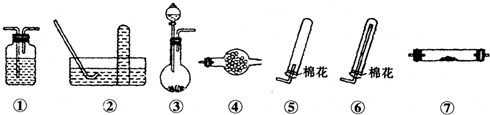
Ⅰ、研究性学习小组进行SO2的制备及性质探究实验,装置如图(a为活塞,加热及固定装置已略去)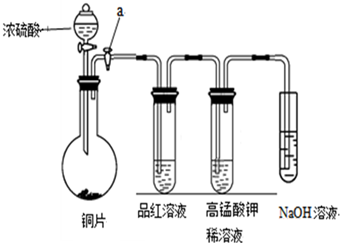
①连接仪器、
②铜与浓硫酸反应的化学方程式是
③从品红溶液中观察到的现象说明SO2具有
④高锰酸钾溶液中的实验现象是
Ⅱ、上述实验中NaOH溶液用于吸收剩余的SO2生成Na2SO3,Na2SO3是抗氧剂.向烧碱和Na2SO3混合溶液中加入少许溴水,振荡后溶液变为无色.
(1)写出在碱性中Br2氧化Na2SO3的离子方程式
(2)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO42-和Br-的实验报告(步骤可增减).限选试剂:2mol?L-1HCl;1mol?L-1 H2SO4;l mol?L-1BaCl2;1 mol?L-1Ba(NO3)2;0.1mol?L-1AgNO3;CCl4;新制饱和氯水.
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 有白色沉淀生成,证明待测液中含SO42-. | |
| 步骤② | ||
| 步骤③ | ||
| … |
分析:Ⅰ、①依据装置制备气体验证气体性质分析步骤;
②铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水;
③依据二氧化硫的漂白性解释;
④二氧化硫通入高锰酸钾溶液中发生氧化还原反应使高锰酸钾溶液褪色;
Ⅱ、(1)Na2SO3和溴发生氧化还原反应;
(2)检验SO42-,可用硝酸酸化的BaCl2;检验Br-,可用氯水,加入四氯化碳后,根据四氯化碳层的颜色进行判断.
②铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水;
③依据二氧化硫的漂白性解释;
④二氧化硫通入高锰酸钾溶液中发生氧化还原反应使高锰酸钾溶液褪色;
Ⅱ、(1)Na2SO3和溴发生氧化还原反应;
(2)检验SO42-,可用硝酸酸化的BaCl2;检验Br-,可用氯水,加入四氯化碳后,根据四氯化碳层的颜色进行判断.
解答:解:Ⅰ、①装置是制备气体的反应,连接好装置需要检验装置的气密性,再加入试剂发生反应;
故答案为:检验装置气密性;
②铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
③二氧化硫具有漂白性,能使品红溶液红色褪去;
故答案为:漂白性;
④二氧化硫具有还原性通入高锰酸钾溶液被氧化为硫酸,高锰酸钾溶液紫红色褪去变化为无色;
故答案为:溶液由紫红色变为无色;
Ⅱ、(1)向烧碱和Na2SO3混合溶液中加入少许溴水,振荡后溶液变为无色,说明亚硫酸根离子被溴单质氧化为硫酸跟,依据电荷守恒和原子守恒配平写出离子方程式为:SO32-+Br2+2 OH-=H2O+SO42-+2Br-;
故答案为:SO32-+Br2+2 OH-=H2O+SO42-+2Br-;
(2)检验SO42-,可取少量待测液加入试管中,加入过量的2 mol?L-1盐酸,再滴加适量l mol?L-1BaCl2溶液;
检验Br-,可取出步骤①中适量上层清液于试管中,加入适量氯水,观察溶液的颜色.(若再加入四氯化碳,振荡,静置后观察颜色也可),或方法2:另取少量待测液加入试管中,加入足量的2 mol?L-1盐酸直到不产生气泡为止,再加入少量氯水,观察溶液的颜色.(若再加入四氯化碳,振荡,静置后观察颜色也可),如溶液呈橙黄色,证明待测液中含Br-.(下层液体呈橙红色,证明待测液中含Br-.)
故答案为:
故答案为:检验装置气密性;
②铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式Cu+2H2SO4(浓)
| ||
故答案为:Cu+2H2SO4(浓)
| ||
③二氧化硫具有漂白性,能使品红溶液红色褪去;
故答案为:漂白性;
④二氧化硫具有还原性通入高锰酸钾溶液被氧化为硫酸,高锰酸钾溶液紫红色褪去变化为无色;
故答案为:溶液由紫红色变为无色;
Ⅱ、(1)向烧碱和Na2SO3混合溶液中加入少许溴水,振荡后溶液变为无色,说明亚硫酸根离子被溴单质氧化为硫酸跟,依据电荷守恒和原子守恒配平写出离子方程式为:SO32-+Br2+2 OH-=H2O+SO42-+2Br-;
故答案为:SO32-+Br2+2 OH-=H2O+SO42-+2Br-;
(2)检验SO42-,可取少量待测液加入试管中,加入过量的2 mol?L-1盐酸,再滴加适量l mol?L-1BaCl2溶液;
检验Br-,可取出步骤①中适量上层清液于试管中,加入适量氯水,观察溶液的颜色.(若再加入四氯化碳,振荡,静置后观察颜色也可),或方法2:另取少量待测液加入试管中,加入足量的2 mol?L-1盐酸直到不产生气泡为止,再加入少量氯水,观察溶液的颜色.(若再加入四氯化碳,振荡,静置后观察颜色也可),如溶液呈橙黄色,证明待测液中含Br-.(下层液体呈橙红色,证明待测液中含Br-.)
故答案为:
| 编号 | 实验操作 | 预期现象和结论 |
| 步骤① | 取少量待测液加入试管中,加入过量的2 mol?L-1盐酸,再滴加适量l mol?L-1BaCl2溶液. | |
| 步骤② | 方法1:取出步骤①中适量上层清液于试管中,加入适量氯水,观察溶液的颜色.(若再加入四氯化碳,振荡,静置后观察颜色也可) | 溶液呈橙黄色,证明待测液中含Br-. (下层液体呈橙红色,证明待测液中含Br-.) |
| 方法2:另取少量待测液加入试管中,加入足量的2 mol?L-1盐酸直到不产生气泡为止,再加入少量氯水,观察溶液的颜色.(若再加入四氯化碳,振荡,静置后观察颜色也可) | 溶液呈橙黄色,证明待测液中含Br-.(下层液体呈橙红色,证明待测液中含Br-.) | |
点评:本题综合考查化学实验放方案的评价,二氧化硫的制备和性质实验严恒方法分析,侧重于学生的实验能力和评价能力的考查,为高考常见题型,注意相关物质的性质的异同,把握实验方案的严密性,难度中等.

练习册系列答案
相关题目
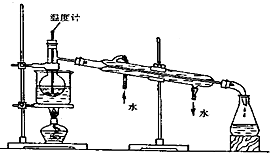
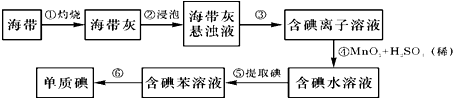
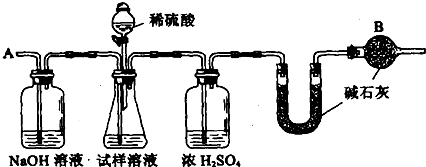
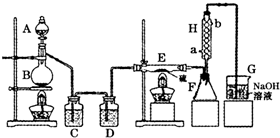
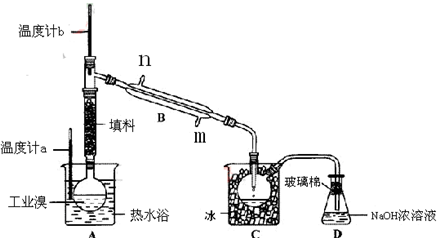 某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃.微溶于水,有毒性和强腐蚀性.他们参观生产过程后,绘制了如下装置简图.
某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃.微溶于水,有毒性和强腐蚀性.他们参观生产过程后,绘制了如下装置简图.