题目内容
【题目】为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取无水氯化铝、绿矾晶体(FeSO47H2O)和胆矾晶体。
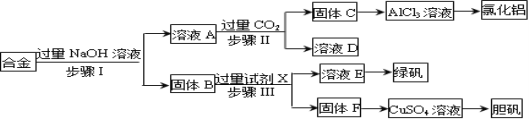
请回答:
【制备无水氯化铝】
(1)步骤Ⅰ进行的实验操作所需要的玻璃仪器是 ;
(2)步骤Ⅱ生成固体C的离子方程式是 ;
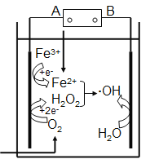
(3)进行步骤Ⅱ时,该小组用如下图所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 ;
(4)由AlCl3溶液制备无水AlCl3的实验过程如下:
①由AlCl3溶液制备氯化铝晶体(AlCl36H2O)涉及的操作为: 、冷却结晶、过滤、洗涤;
②将AlCl36H2O溶于浓硫酸进行蒸馏,可以得到一定量的无水AlCl3,此原理是利用浓硫酸下列性质中的 (填字母)。
a.氧化性 b.吸水性 c.难挥发性 d.脱水性
【制备胆矾晶体】
(5)用固体F制备CuSO4溶液,可设计以下三种途径,你认为的最佳途径为 。(填序号)


【测定FeSO47H2O含量】
(6)称取制得的绿矾样品10.0 g,溶于适量的稀硫酸中,配成100 mL溶液,准确量取25.00 mL该液体于锥形瓶中,再用0.1000 mol/L KMnO4标准溶液滴定。用同样的方法滴定3次,平均消耗15.00 mL标准液,则样品中FeSO47H2O的质量分数为 。(已知Mr(FeSO4·7H2O)=278)
【答案】(1)漏斗、烧杯、玻璃棒(2)AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-
(3)在装置a、b之间增加一个盛有饱和NaHCO3溶液的洗气瓶(合理即可) (4)①蒸发浓缩
②b c(5)②(6)83.4%
【解析】
试题分析:铝、铁和铜的合金中只有金属铝可以和氢氧化钠之间反应生成溶液A偏铝酸钠,固体B是金属铁和金属铜,A中通入过量的二氧化碳可以得到氢氧化铝沉淀C和碳酸氢钠溶液D,金属铁可以和硫酸之间发生反应生成硫酸亚铁和氢气,但是金属铜和稀硫酸之间不反应,硫酸亚铁溶液蒸发浓缩、冷却结晶可以获得绿矾晶体,金属铜可以获得胆矾晶体。
(1)步骤Ⅰ进行的实验操作是过滤,所需要的玻璃仪器是漏斗、烧杯、玻璃棒;
(2)根据以上分析可知步骤Ⅱ生成固体C的离子方程式是AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-。
(3)进行步骤Ⅱ时,该小组用如图2所示装置及试剂将制得的CO2气体通入溶液A中.一段时间后,观察到烧杯中产生的白色沉淀逐渐减少,其原因是二氧化碳气体中含有从盐酸中挥发出的氯化氢气体,氯化氢在水中溶解了部分沉淀氢氧化铝,发生的反应为Al(OH)3+3H+=Al3++3H2O,为了避免固体C减少,可在制取二氧化碳的收集装置中增加一个洗去氯化氢的装置,二氧化碳在饱和碳酸氢钠中不溶,氯化氢和碳酸氢钠反应生成二氧化碳气体,所以可在装置I和Ⅱ之间增加一个盛有饱和碳酸氢钠溶液的洗气瓶,除去二氧化碳中的氯化氢;
(4)①由AlCl3溶液制备氯化铝晶体(AlCl36H2O)涉及的操作为蒸发浓缩、冷却结晶、过滤、洗涤;
②浓硫酸具有吸水性和难挥发性,因此将AlCl36H2O溶于浓硫酸进行蒸馏,可以得到一定量的无水AlCl3。
(5)金属铜可以和硝酸之间反应生成硝酸铜、一氧化氮和水,即3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O,铜不能和稀硫酸反应,但是当加热并通入空气之后,铜和氧气反应生成氧化铜,然后氧化铜会和硫酸反应生成硫酸铜,不会产生污染大气的气体,该过程原料利用率高,所以途径②最佳。
(6)根据电子得失守恒可知样品中FeSO47H2O的质量分数为
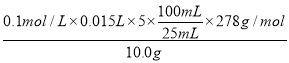 ×100%=83.4%。
×100%=83.4%。

 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案