题目内容
1.现代科技证明,葡萄酒中含有的白藜芦醇具有美容养颜之功效.下列关于白藜芦醇 (C14H12O3)的说法错误的是( )| A. | 每个白藜芦醇分子中含有6个氢分子 | |
| B. | 白藜芦醇由碳、氢、氧三种元素组成 | |
| C. | 白藜芦醇的相对分子质量为228 | |
| D. | 白藜芦醇中碳、氢、氧三种元素的质量比为14:12:3 |
分析 A.由分子式判断分子中H原子数;
B.由分子式判断组成元素;
C.相对分子质量为构成分子的各原子的相对原子质量之和;
D.化合物中各元素质量比=各原子的相对原子质量×原子个数之比.
解答 解:A.由分子式C14H12O3可知分子中H原子数为12,故A错误;
B.由分子式C14H12O3可知白藜芦醇由碳、氢、氧三种元素组成,故B正确;
C.相对分子质量为构成分子的各原子的相对原子质量之和,则白藜芦醇的相对分子质量为12×14+1×12+16×3=228,故C正确;
D.化合物中各元素质量比=各原子的相对原子质量×原子个数之比=(12×14):(1×12):(16×3)=14:1:4,故D错误.
故选AD.
点评 本题考查有机物的结构与组成,题目难度不大,侧重于基础知识的考查,注意根据题目中所给的分子式分析.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.下列关于化学用语的表示正确的是( )
| A. | 二氟化氧分子电子式: | |
| B. | 质子数与中子数相等的硫原子${\;}_{16}^{16}$S | |
| C. | 镁离子的结构示意图: | |
| D. | 对甲基苯酚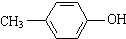 |
12.将过量Na2O2固体加入到Ca(HCO3)2溶液中,下列有关说法正确的是( )
| A. | 溶液中只有气体产生 | |
| B. | 溶液中只有沉淀产生 | |
| C. | 溶液中有反应:Ca2++OH-+HCO-3═CaCO3↓+H2O发生 | |
| D. | 溶液中有反应:Ca2++2OH-+2HCO-3═CaCO3↓+CO32-+2H2O发生 |
13.下列说法或表示方法正确的是( )
| A. | 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 | |
| B. | 由C(金刚石)═C(石墨)△H=-1.9kJ/mol 可知,金刚石比石墨稳定 | |
| C. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的稀溶液混合,放出的热量大于57.3 kJ | |
| D. | 在25℃、101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 |
11. 某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
Ⅰ.配制0.50mol•L-1 NaOH溶液
若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体5.0g
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.
取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
①表中的温度差平均值为4.0℃
②近似认为0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容c=“4.18“J•(g•℃)-1.则该反应的热化学方程式为$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-53.5kJ/mol(计算取小数点后一位).
③上述实验数值结果与57.3kJ•mol-1有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.所用硫酸为浓硫酸
c.环形玻璃搅拌棒改为铜质搅拌棒
d.倒完NaOH溶液后,发现装NaOH烧杯内有极少量残留液.
 某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.
某实验小组用0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液进行中和热的测定.Ⅰ.配制0.50mol•L-1 NaOH溶液
若实验中大约要使用245mL NaOH溶液,至少需要称量NaOH固体5.0g
Ⅱ.测定稀硫酸和稀氢氧化钠中和热的实验装置如图所示.
取50mL NaOH溶液和30mL硫酸溶液进行实验,实验数据如表.
| 温度 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | 温度差 平均值 (t2-t1)/℃ | ||
| H2SO4 | NaOH | 平均值 | |||
| 1 | 26.2 | 26.0 | 26.1 | 30.1 | |
| 2 | 27.0 | 27.4 | 27.2 | 33.3 | |
| 3 | 25.9 | 25.9 | 25.9 | 29.8 | |
| 4 | 26.4 | 26.2 | 26.3 | 30.4 | |
②近似认为0.50mol•L-1NaOH溶液和0.50mol•L-1硫酸溶液的密度都是1g•cm-3,中和后生成溶液的比热容c=“4.18“J•(g•℃)-1.则该反应的热化学方程式为$\frac{1}{2}$H2SO4(aq)+NaOH(aq)=$\frac{1}{2}$Na2SO4(aq)+H2O(l)△H=-53.5kJ/mol(计算取小数点后一位).
③上述实验数值结果与57.3kJ•mol-1有偏差,产生偏差的原因可能是(填字母)acd.
a.实验装置保温、隔热效果差
b.所用硫酸为浓硫酸
c.环形玻璃搅拌棒改为铜质搅拌棒
d.倒完NaOH溶液后,发现装NaOH烧杯内有极少量残留液.
 由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去).
由短周期元素组成的中学常见无机物A、B、C、D、E、X存在如图转化关系(部分生成物和反应条件略去). ;
;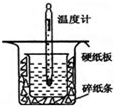 (1)用 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
(1)用 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题: