题目内容
【题目】实验室要配制100mL、10molL-1的NaCl溶液,试回答下列各题:
(1)经计算,应该用托盘天平称取NaCl固体___g。
(2)配制溶液时一般可分为以下几个步骤:①称量②计算③定容④移液⑤洗涤⑥溶解其正确的操作顺序为(填编号)___。
(3)容量瓶上需标有以下5项中的___
①温度 ②浓度 ③容量 ④压强 ⑤刻度线
A.①②④ B.③⑤⑥ C.①③⑤ D.②④⑥
(4)若用NaCl固体配制溶液,下列仪器中,不需要用到的是___。(填序号)
A.蒸发皿 B.100mL容量瓶 C.烧杯 D.胶头滴管 E.药匙 F.托盘天平 G.玻璃棒
(5)下列错误操作会导致所得溶液偏低的是___(多项,填序号)。
A.定容时仰视容量瓶刻度线区
B.容量瓶中原有少量蒸馏水
C.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处
D.配制好溶液后,容量瓶未塞好,酒出一些溶液
【答案】58.5 ②①⑥④⑤③ C A AC
【解析】
(1)根据m=nM=cVM计算;
(2)配制一定物质的量浓度溶液的步骤为:计算、称量、溶解、转移、洗涤、定容,据此排序;
(3)容量瓶上标有刻度线、温度、容量,据此分析判断;
(4)若用NaCl固体配制溶液,需用药匙取药品、托盘天平称量药品、烧杯溶解药品、玻璃棒搅拌和引流、胶头滴管定容、100mL容量瓶配制溶液,据此判断不需要的仪器;
(5)根据c=![]() 知,如果n偏小或V偏大都导致配制溶液浓度偏低,据此分析判断。
知,如果n偏小或V偏大都导致配制溶液浓度偏低,据此分析判断。
(1)应该用托盘天平称取NaCl固体的质量m=cVM=10mol/L×0.1L×58.5g/mol=58.5g,故答案为:58.5;
(2)配制一定物质的量浓度溶液的步骤为:计算、称量、溶解、转移、洗涤、定容,所以配制溶液时步骤②①⑥④⑤③,故答案为:②①⑥④⑤③;
(3)容量瓶上标有温度、容量和刻度线,故选C;
(4)若用NaCl固体配制溶液,需用药匙取药品、托盘天平称量药品、烧杯溶解药品、玻璃棒搅拌和引流、胶头滴管定容、100mL容量瓶配制溶液,所以不需要的仪器是蒸发皿,故选A;
(5)A.定容时仰视容量瓶刻度线,会导致溶液的体积偏大,配制溶液的浓度偏低,故A正确;B.容量瓶中原有少量蒸馏水,不影响溶液的体积和溶质的物质的量,配制的溶液浓度无影响,故B错误;C.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处,导致溶液的体积偏大,配制溶液的浓度偏低,故C正确;D.配制好溶液后,容量瓶未塞好,洒出一些溶液,溶液的浓度不变,故D错误;故选AC。

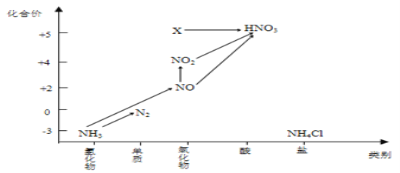
【题目】硫代硫酸钠(Na2S2O3)可用作分析试剂、基准试剂、还原剂、除氯剂等。
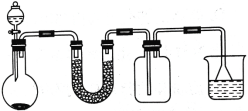
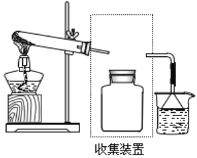
Ⅰ、实验室制备硫代硫酸钠装置图如下。

(1)仪器B的名称是________。
(2)写出装置B制备Na2S2O3的化学反应方程式____________________________。
(3)NaOH溶液的作用是____________________________________。
Ⅱ、测硫代硫酸钠样品纯度步骤如下
①称取Ⅰ中制得硫代硫酸钠样品8.0g配成250mL溶液
②从①中量取20.00mL溶液于锥形瓶中
③用0.lmol·L-1标准碘液滴定,实验测得数据如下
滴定前读数(mL) | 滴定后读数(mL) | 待测液体积(mL) | |
实验一 | 1.20 | 21.00 | 20.00 |
实验二 | 0.40 | 19.20 | 20.00 |
实验三 | 0.50 | x | 20.00 |
(4)该滴定时,向锥形瓶中加入1至2滴淀粉液作指示剂,则达到滴定终点的判断标准是______________。
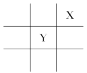
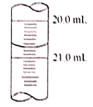
(5)x读数如图所示,则x=________,根据所测的数据计算该硫代硫酸钠样品纯度为_______________。(已知I2+2Na2S2O3=2NaI+Na2S4O6)
(6)若步骤①中量取20.00mL硫代硫酸钠溶液时,未用硫代硫酸钠溶液润洗滴定管,则测得样品的纯度将______________(填“偏大”或“偏小”)。