题目内容
【题目】根据下列实验操作和现象得出的结论正确的是
操作 | 现象 | 结论 | |
A | 将 | 溴水和酸性高锰酸钾溶液均褪色 |
|
B | 向 | 先产生白色沉淀,后产生红褐色沉淀 |
|
C | 向滴有酚酞的 | 有白色沉淀生成,溶液红色变浅 |
|
D | 将 | 产生白色沉淀 | 酸性: |
A.AB.BC.CD.D
【答案】C
【解析】
A.将![]() 分别通人溴水和酸性高锰酸钾溶液中,溴水和酸性高锰酸钾溶液均褪色,体现了SO2的还原性,而不是漂白性,故A错误;
分别通人溴水和酸性高锰酸钾溶液中,溴水和酸性高锰酸钾溶液均褪色,体现了SO2的还原性,而不是漂白性,故A错误;
B.向![]() 溶液中滴加1~2滴
溶液中滴加1~2滴![]() 溶液,再滴加2滴
溶液,再滴加2滴![]() 溶液,观察到先产生白色沉淀,后产生红褐色沉淀,因NaOH溶液过量,无法判断
溶液,观察到先产生白色沉淀,后产生红褐色沉淀,因NaOH溶液过量,无法判断![]() ,故B错误;
,故B错误;
C.向滴有酚酞的![]() 溶液中加入少量
溶液中加入少量![]() 固体,发现有有白色沉淀生成,溶液红色变浅,说明Ba2+与CO32-结合生成BaCO3沉淀,促进CO32-的水解平衡逆向移动,溶液的碱性减弱,故C正确;
固体,发现有有白色沉淀生成,溶液红色变浅,说明Ba2+与CO32-结合生成BaCO3沉淀,促进CO32-的水解平衡逆向移动,溶液的碱性减弱,故C正确;
D.将![]() 与盐酸反应得到的气体直通入
与盐酸反应得到的气体直通入![]() 溶液中,观察到产生白色沉淀,因盐酸有挥发性,生成的CO2中混有HCl,则无法判断碳酸的酸性比硅酸强,故D错误;
溶液中,观察到产生白色沉淀,因盐酸有挥发性,生成的CO2中混有HCl,则无法判断碳酸的酸性比硅酸强,故D错误;
故答案为C。

练习册系列答案
相关题目
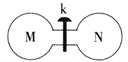
【题目】常温下,向如图所示的两个容积相同的刚性容器中分别充入气体M、N(如表所示),使两容器中压强相等。打开开关k,两容器中的气体充分混合后,恢复至常温,容器内的气体压强(固体影响忽略不计)由大到小的顺序正确的是 ( )
装置 | 编号 |
|
|
|
|
| M | NH3 | HI | NO | H2 |
N | Cl2 | Cl2 | O2 | O2 |
A.①=④>②=③ B.①=④>②>③
C.④>①>②>③D.①>④>②>③