��Ŀ����
����Ŀ��һ�������£���3molA��1molB�����������ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A(g)+B(g) ![]() xC(g)+2D(s)��2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.2mol/L�������ж���ȷ����
xC(g)+2D(s)��2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.2mol/L�������ж���ȷ����
A���ӿ�ʼ��ƽ��A��ƽ����Ӧ����Ϊ0.3mol/(L![]() s)
s)
B���ӿ�ʼ��ƽ��B��ת����Ϊ60%
C���˷�Ӧ�Ļ�ѧƽ�ⳣ������ʽ![]()
D�������������ܶȲ��ٸı�ʱ���÷�Ӧһ���ﵽƽ��״̬
���𰸡�D
��������
���������һ�������£���3molA��1molB�����������ڹ̶��ݻ�Ϊ2L���ܱ������У��������·�Ӧ��3A(g)+B(g)![]() xC(g)+2D(s)��2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.2mol/L�����ݻ�ѧƽ������ʽ��ʽ���㣻
xC(g)+2D(s)��2minĩ�÷�Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.2mol/L�����ݻ�ѧƽ������ʽ��ʽ���㣻
3A(g)+B(g)![]() xC(g)+2D(s)
xC(g)+2D(s)
��ʼ��(mol) 3 1 0 0
�仯��(mol) 1.2 0.4 0.4x 0.8
ƽ����(mol) 1.8 0.6 0.4x 0.8
C��Ũ��Ϊ0.2mol/L��C�����ʵ���Ϊ0.4������õ�x=1��A��A��ƽ����Ӧ����=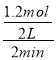 =0.3mol/(Lmin)����A����B��B��ת����=
=0.3mol/(Lmin)����A����B��B��ת����=![]() ��100%=40%����B����C��DΪ���壬�������´˷�Ӧ�Ļ�ѧƽ�ⳣ��=
��100%=40%����B����C��DΪ���壬�������´˷�Ӧ�Ļ�ѧƽ�ⳣ��=![]() ����C����D����Ӧ�������к��й��壬�ܶȵ�����������������������������������ܶȲ��ٸı�ʱ���÷�Ӧһ���ﵽƽ��״̬����D��ȷ����ѡD��
����C����D����Ӧ�������к��й��壬�ܶȵ�����������������������������������ܶȲ��ٸı�ʱ���÷�Ӧһ���ﵽƽ��״̬����D��ȷ����ѡD��

 ��У���˿��ֿ���ϵ�д�
��У���˿��ֿ���ϵ�д�����Ŀ����֪��ӦH2��g��+ I2��g��![]() 2HI��g����1 mol H2��ȫ��Ӧ�ų�a kJ�������������±����ݣ�����˵������������ ��
2HI��g����1 mol H2��ȫ��Ӧ�ų�a kJ�������������±����ݣ�����˵������������ ��
�� ѧ �� | H��H | I��I |
�Ͽ�1 mol��ѧ��ʱ���յ�������kJ�� | b | c |
A���÷�Ӧ�з�Ӧ��������������������������
B���Ͽ�1 mol H-H ����1 mol I-I �������������ڶϿ�2 mol H-I ����������
C���Ͽ�2 mol H-I����������Ϊ��a+b+c��kJ
D�����ܱ������м���2 mol H2��2 mol I2����ַ�Ӧ��ų�������С��2a kJ
����Ŀ��ij�¶�ʱ����2 L�ܱ������У�������̬����X��Y��Z�����ʵ�����n����ʱ�䣨t���仯��������ͼ��ʾ����ͼ�����ݷ����ɵã�
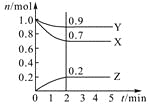
��1���÷�Ӧ�Ļ�ѧ����ʽΪ ��
��2����Ӧ��ʼ��2 min����Y��ʾ��ƽ����Ӧ����Ϊ ��X��ת����Ϊ ��
��3����һ���¶��£������������Ϊ������Ӧ�ﵽ��Ӧ�ȵı�־���� ��
A��X��Y��Z��Ũ����� |
B��X��Y��Z�ķ�������Ϊ3�U1�U2 |
C��Z������������Y���������ʵĶ��� |
D����λʱ��������n mol Y��ͬʱ����3n mol X |
��4�����ܱ������ͨ��a mol A��g����b mol B��g����
������ӦA��g��+ B��g��= 2C��g�������ı���������ʱ����ӿ췴Ӧ���ʵ��� ������ţ���
�������¶�
������������������䣬���뺤��
���������
������������������䣬����A��g�������ʵ���